par Klqsen » 07 Nov 2017, 12:17
par Klqsen » 07 Nov 2017, 12:17
Salut,
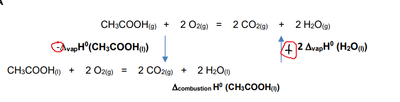
Dans le QCM on nous donne CH3COOH sous forme gazeuse et de même pour H2O. Sauf que dans notre résultat de l'enthalpie de combustion, on à CH3COOH sous forme liquide et la même chose pour H2O.
Du coup, pour passé de CH3COOH (g) à CH3COOH (l) on doit utiliser l'enthalpie de vaporisation de CH3COOH que l'on nous donne, ici 150 kJ/mol.
Ce que je ne comprends pas c'est pourquoi de CH3COOH (g) à CH3COOH (l) on a -150 kJ/mol dans la correction ?
Merci !
PS : Du coup je pense avoir compris ! En faite pour passer de gazeux à liquide, c'est une liquéfaction or on nous donne le contraire, on nous donne la vaporisation. Vu que l'on veut la réaction inverse à la vaporisation bah on met un (-) devant. C'est pour ça qu'il y a le - devant 150 (sur l'image)
- Fichiers joints
-