Zhost a écrit:Coucou ^^.
J'me suis posé une question euh... inutile ^^.
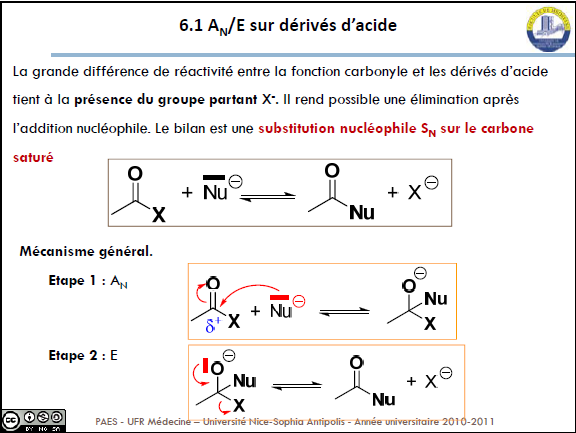
On sait très bien que le chlorure d'acyle n'a pas besoin de catalyse acide pour former un acide carboxylique en présence d'H2O. (ce qui est contraire du cas de l'amide, du nitrile et de l'ester).
Mais, si on met une catalyse acide, qu'est-ce qui se passe ?
J'ai pensé à une activation électrophile sur l'oxygène. Et après le OH- du H2O fait une attaque nucléophile, la double liaison remonte et le chlore s'expulse car il se sentira plus réactif avec l'hydrogène seul.
Donc au final je me retrouve avec un diol géminé.
Yop !
Je suis d'accord pour l'activation électrophile. Par contre après, je pense que c'est plutôt une attaque nucléophile du H2O "entier" (pourquoi OH- ?) sur le carbone-électrophile qu'on vient de créer (double effet inductif attracteur super-power rose et bleu). Puis l'H2O+ va lâcher un de ses protons au chlore, qui a plein de doublets non-liants pour lui dire "viens !". Lorsque la double liaison C=O revient en place, un H+ est libéré dans le milieu (catalyse) et on dégage un HCl, on a alors HCl, l'acide carboxylique et un H+ au final.
Au final, même résultat, c'est juste que le carbone est déjà très électrophile à la base à cause de l'effet inductif du chlore, alors pas besoin d'activation électrophile de l'oxygène.
Bon je suis pas sûr du tout mais ça parait plausible o_o
Zhost a écrit:Et aussi, dans le même truc, je me pose une question quant à la compétitivité de la catalyse acide sur l'azote ou l'oxygène de l'amide.
Qu'est-ce qui forcerait à ce que l'H+ attaque l'amide entrainant son expulsion plutôt que l'oxygène ?
Est-ce principalement du aux effets inductifs donneurs que reçoit l'azote ?
Merci

!
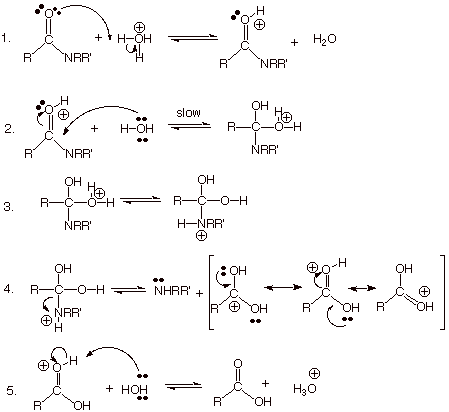
Justement, il attaque l'oxygène ! Le DNL de l'azote est dans une mésomérie, il est pas facile à attaquer .
En gros :
H2O arrive sur le carbone nucléophile formé, on se retrouve avec C—H2O+.
H2O+ lâche un proton à l'azote qui devient NH
3+ ou NH
2R+ ou NHR
2+ (selon l'amide que tu as au départ). En effet ici il n'y a plus mésomérie puisqu'on a choppé la liaison π de l'oxygène.
La liaison C—N+ se rabat (instable) et un DNL de l'oxygène se rabat pour faire C=OH+.
Le H+ de C=OH+ va dégager et on retrouve notre proton catalytique ainsi qu'une amine et un acide carboxylique.
J'espère avoir été clair et juste (c'est mieux quand c'est juste)!
PS : j'ai trouvé ça pour illustrer, car a l'écrit ça a pas beaucoup de sens !! EDIT : meilleur mécanisme =D