Le Guide pour bien débuter la LAS : Ici
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Différence molécule polaire / non polaire
4 messages
• Page 1 sur 1
Différence molécule polaire / non polaire
Bonjour a tous  , je pense que c'est débile mais je ne me souviens plus quelle est la difference entre une molécule polaoire et non polaire. Merci beaucoup d'avance
, je pense que c'est débile mais je ne me souviens plus quelle est la difference entre une molécule polaoire et non polaire. Merci beaucoup d'avance 
-

valou - Carabin newbie
- Messages: 14
- Inscription: 05 Aoû 2011, 21:44
Re: Différence molécule polaire / non polaire
Molécule polaire signifie que les barycentres de tes charges positives et négatives de la molécule ne correspondent pas ( ils ne sont pas au meme endroit )
Molécule non polaire : les barycentres sont au même endroit

Molécule non polaire : les barycentres sont au même endroit
-

Sam - Tut' Biophy/Physique

- Messages: 505
- Inscription: 29 Sep 2010, 15:54
Re: Différence molécule polaire / non polaire
Merci beaucoup 
-

valou - Carabin newbie
- Messages: 14
- Inscription: 05 Aoû 2011, 21:44
Re: Différence molécule polaire / non polaire
Salut ! 
Une molécule polaire a ses 2 barycentres (positifs et négatifs) distincts, donc 2 pôles, un positif et un négatif.
Cela est dû à l'électronégativité des atomes, les plus électronégatifs ont tendance à attirer les électrons de la liaison vers eux, ce qui fait que t'as une concentration de charges négatives d'un côté, et une concentration de charges positives de l'autre.
Un exemple : le bromure d'hydrogène (HBr), le Br est plus électronégatif, il veut devenir Br- et va donc attirer les 2 électrons qui forment la liaison entre ces 2 atomes ; le H au contraire n'est pas (ou très peu) électronégatif (il devient d'ailleurs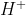 et non
et non  ). On aura donc le barycentre des charges positives prêt du H et le barycentre des charges négatives prêt du Br.
). On aura donc le barycentre des charges positives prêt du H et le barycentre des charges négatives prêt du Br.
La polarité peut être accentuée par la forme géométrique de la molécule ( est coudée, le barycentre des charges positives est entre les H et le barycentre des charges négatives prêt du O).
est coudée, le barycentre des charges positives est entre les H et le barycentre des charges négatives prêt du O).
Pour une molécule non polaire, les barycentres sont confondus, c'est le cas des molécules symétriques et linéaires (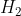 ,
, 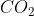 , etc...).
, etc...).
Tu verras cette notion en profondeur en Chimie G et Chimie Orga ++
C'est clair ?
EDIT : doublé par Sam, tant pis pour la double explication, dommage d'effacer
EDIT 2 : décidément, doublé par Valou aussi... du coup ça devient inutile de poster... xD (au cas où, si quelqu'un n'a toujours pas compris...)
Une molécule polaire a ses 2 barycentres (positifs et négatifs) distincts, donc 2 pôles, un positif et un négatif.
Cela est dû à l'électronégativité des atomes, les plus électronégatifs ont tendance à attirer les électrons de la liaison vers eux, ce qui fait que t'as une concentration de charges négatives d'un côté, et une concentration de charges positives de l'autre.
Un exemple : le bromure d'hydrogène (HBr), le Br est plus électronégatif, il veut devenir Br- et va donc attirer les 2 électrons qui forment la liaison entre ces 2 atomes ; le H au contraire n'est pas (ou très peu) électronégatif (il devient d'ailleurs
La polarité peut être accentuée par la forme géométrique de la molécule (
Pour une molécule non polaire, les barycentres sont confondus, c'est le cas des molécules symétriques et linéaires (
Tu verras cette notion en profondeur en Chimie G et Chimie Orga ++
C'est clair ?
EDIT : doublé par Sam, tant pis pour la double explication, dommage d'effacer
EDIT 2 : décidément, doublé par Valou aussi... du coup ça devient inutile de poster... xD (au cas où, si quelqu'un n'a toujours pas compris...)
-

P-A - Carabin addicted
- Messages: 1302
- Inscription: 21 Juil 2010, 12:22
4 messages
• Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum: Aucun utilisateur enregistré et 0 invités