Coucou !
Je vais essayer de tout reprendre

Du coup un electron est défini par 4 nombres quantiques (n, l, m et s)
- Le n c'est la niveau d'énergie (et la chiffre avant la lettre quand tu écrit la configuration électronique)
- Le l définit le sous niveau énergétique (et la petite lettre dans les configuration électronique) mais aussi le nombre de cases quantiques (par exemple, pour s --> 1 case, p --> 3 cases, d --> 5 cases, ....)
- Le m définit les cases quantique (avec un nombre compris entre -l et +l)
Du coup ici, ce qui nous intéresse, c'est le m=0 !
On commence par écrire la configuration électronique de l'atome
Puis, on représente les électrons et les cases quantiques (avec le tableau qui est dans la correction) en faisant correspondre chaque case à son m correspondant (pour s on a m=0, pour p m= -1, 0 ou 1, ...)
Une fois tous les électrons mis (en respectant bien toutes les règles), il reste plus qu'à compter et on obtient 16

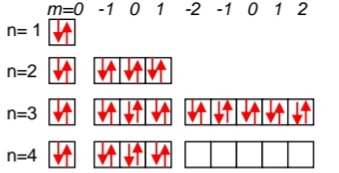
- Screenshot_20220121-221717_OneDrive.jpg (19.44 Kio) Vu 236 fois
Dit moi s'il y a un point qui est moins clair, j'essayerai de le détailler plus






 Chef Tut' Orientation et Réorientation 2022-2023
Chef Tut' Orientation et Réorientation 2022-2023 
 Tuteur de Chimie (ECUE11) 2021-2022
Tuteur de Chimie (ECUE11) 2021-2022 
 Ronéiste de Chimie 2021-2022
Ronéiste de Chimie 2021-2022 



 Tuteur de Chimie 2021/2022
Tuteur de Chimie 2021/2022 


