Bonsoir à tous,
Petite difficulté sur la VSEPR : a été donné en cours 2 exemples
1 Méthyl donc 1 Carbonne entouré de 4 Hydrogènes
=> A X4 E0 c'est compréhensible
ensuite 2 Oxugènes avec une double liaison ( O=O )
et la, Michael, tu as marqué
=> A X1 E2 : X1 ok car tu as dis que la double liaison compte 1, mais pourquoi E2 ? Car il me semble qu'il y a 2 x 2 doublets non-liants, non ?
Le Guide pour bien débuter la LAS : Ici
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
INSCRIPTIONS ATELIERS ORAUX : Ici
SUJETS EB SEMESTRE 2 : Ici
Newsletter : ICI
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
INSCRIPTIONS ATELIERS ORAUX : Ici
SUJETS EB SEMESTRE 2 : Ici
Newsletter : ICI
la VSEPR
9 messages
• Page 1 sur 1
Re: la VSEPR
Hey!
Nan je me suis pas trompé mais je me suis peut être mal expliqué: quand tu fais la VSEPR tu fais pas la VSEPR d'une molécule mais la VSEPR d'un atome choisi.
Pour le méthane j'ai fais la VSEPR de l'atome de carbone au centre (il fais 4 liaisons et il a aucun doublet non-liant) et pour le dioxygnène j'ai fais la VSEPR d'un des deux atomes d'oxygènes (qui a bien 2 doublets non-liant)! Je l'ai peut être pas super bien expliqué parce que du coup les 2 atomes d'oxygène ont la même VSEPR.
par exemple dans la molécule de méthane j'aurais très bien pu faire la VSEPR d'un des atomes d'hydrgènes (sauf que ça a aucun intérêt)! Ce qui donne du coup AX1E0 (car l'hydrogène fait une liaison avec le carbone et n'a aucun doublet non-liant).
Voilou!
Nan je me suis pas trompé mais je me suis peut être mal expliqué: quand tu fais la VSEPR tu fais pas la VSEPR d'une molécule mais la VSEPR d'un atome choisi.
Pour le méthane j'ai fais la VSEPR de l'atome de carbone au centre (il fais 4 liaisons et il a aucun doublet non-liant) et pour le dioxygnène j'ai fais la VSEPR d'un des deux atomes d'oxygènes (qui a bien 2 doublets non-liant)! Je l'ai peut être pas super bien expliqué parce que du coup les 2 atomes d'oxygène ont la même VSEPR.
par exemple dans la molécule de méthane j'aurais très bien pu faire la VSEPR d'un des atomes d'hydrgènes (sauf que ça a aucun intérêt)! Ce qui donne du coup AX1E0 (car l'hydrogène fait une liaison avec le carbone et n'a aucun doublet non-liant).
Voilou!
-

Micha - Ex-Chef TuT'
- Messages: 203
- Inscription: 12 Juil 2009, 22:37
Re: la VSEPR
Merci beaucoup, c'est noté : la VSEPR ne se fait que pour 1 atome !
- JB [18]
- Carabin newbie
- Messages: 6
- Inscription: 17 Sep 2009, 19:32
Re: la VSEPR
coucou!
J'ai compris comment faire la vsepr, mais j'ai du mal à trouver le nombre de doublet non liants...es-ce qu'on doit les trouver en fesant l'ordre de remplissage et voir dans les orbitales où se trouve les derniers dnl, ou alors y-a t-il une autre méthode? Paske aparament elle ne marche pas tout le temps :/ Par exemple pour le N de NH3 ça donne AX3E (d'après la correc du CB) mais je vois pas où est le dnl!
Donc si quelqu'un peut me dire...
J'ai compris comment faire la vsepr, mais j'ai du mal à trouver le nombre de doublet non liants...es-ce qu'on doit les trouver en fesant l'ordre de remplissage et voir dans les orbitales où se trouve les derniers dnl, ou alors y-a t-il une autre méthode? Paske aparament elle ne marche pas tout le temps :/ Par exemple pour le N de NH3 ça donne AX3E (d'après la correc du CB) mais je vois pas où est le dnl!
Donc si quelqu'un peut me dire...
-

pou² - Apprenti Carabin
- Messages: 129
- Inscription: 21 Sep 2009, 18:30
Re: la VSEPR
Salut!
Alors pour connaitre le nombre de doublets non liant, soit tu dois faire ta configuration électronique et compter le nombre de doublets sur ta couche de valence soit tu le situes dans le tableau périodique pour connaitre sa couche de valence.
Bon après on va pas se le cacher, ça prend 3 ans de faire comme ça! En plus, tu vas voir c'est plus ou moins toujours les mêmes atomes qui ressortent!
Concrètement ce que tu fais, c'est que tu te souviens que l'azote a un doublet, le carbone aucun, l'oxygène 2 et là tu peux en faire déjà pas mal! Ceci dit si tu tombes sur des atomes que tu ne connais pas, tu dois passer par la configuration électronique pour trouver le nombre de dnl.
Pour ton exemple du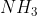 , on te demande la VSEPR de l'azote ==> 3 liaisons + 1 doublets non liants (couche de valence =
, on te demande la VSEPR de l'azote ==> 3 liaisons + 1 doublets non liants (couche de valence =  )! On a donc bien un
)! On a donc bien un  .
.
Voilà j'espère t'avoir aidé à comprendre le truc!
Alors pour connaitre le nombre de doublets non liant, soit tu dois faire ta configuration électronique et compter le nombre de doublets sur ta couche de valence soit tu le situes dans le tableau périodique pour connaitre sa couche de valence.
Bon après on va pas se le cacher, ça prend 3 ans de faire comme ça! En plus, tu vas voir c'est plus ou moins toujours les mêmes atomes qui ressortent!
Concrètement ce que tu fais, c'est que tu te souviens que l'azote a un doublet, le carbone aucun, l'oxygène 2 et là tu peux en faire déjà pas mal! Ceci dit si tu tombes sur des atomes que tu ne connais pas, tu dois passer par la configuration électronique pour trouver le nombre de dnl.
Pour ton exemple du
Voilà j'espère t'avoir aidé à comprendre le truc!
-

Micha - Ex-Chef TuT'
- Messages: 203
- Inscription: 12 Juil 2009, 22:37
Re: la VSEPR
Ouai super micha, ac ça je devrais m'en sortir 
MErci bcp!!
MErci bcp!!
-

pou² - Apprenti Carabin
- Messages: 129
- Inscription: 21 Sep 2009, 18:30
Re: la VSEPR
salut !
comment on trouve LE 3 liaison et LE 1 doublet non liant
la méthode ??!!
merci d'avance
comment on trouve LE 3 liaison et LE 1 doublet non liant
la méthode ??!!
merci d'avance
- ben83
- Carabin newbie
- Messages: 17
- Inscription: 22 Sep 2009, 15:17
Re: la VSEPR
Oyé oyé brave gens!!!
Ben euuu c'est expliqué XD .
Dans cette molécule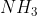 , tu dois trouver la VSEPR du N
, tu dois trouver la VSEPR du N
Donc tu fais ta configuration électronique et tu trouves la couche de valence :
Tu comptes le nombre d'électrons de valence (car ce sont eux qui vont pouvoir faire des liaisons avec les autres élements!!!) . Ici tu en trouves 5 (2+3=5

 )
)
Donc tu as 5 électrons de valence, et tu as dans cette molécule 3 atomes d'H . Un électron de chaque hydrogène va se lier avec un des électrons de N . Donc 3 de tes électrons vont être liés . D'où le .
.
Cependant, tu vois qu'il te reste deux électrons (tout triste de pas avoir trouver d'ami

 ) et donc ils vont faire ami-ami et vont se lier ensemble (que c'est MIGNON ) et former un doublet non liant !!!
) et donc ils vont faire ami-ami et vont se lier ensemble (que c'est MIGNON ) et former un doublet non liant !!!
Et donc on obtient .
.
Voilà après j'espère que c'était ça ta question, parceque bon Micha avait quand même super bien expliqué ^^
Ben euuu c'est expliqué XD .
Dans cette molécule
Donc tu fais ta configuration électronique et tu trouves la couche de valence :
Tu comptes le nombre d'électrons de valence (car ce sont eux qui vont pouvoir faire des liaisons avec les autres élements!!!) . Ici tu en trouves 5 (2+3=5
Donc tu as 5 électrons de valence, et tu as dans cette molécule 3 atomes d'H . Un électron de chaque hydrogène va se lier avec un des électrons de N . Donc 3 de tes électrons vont être liés . D'où le
Cependant, tu vois qu'il te reste deux électrons (tout triste de pas avoir trouver d'ami
Et donc on obtient
Voilà après j'espère que c'était ça ta question, parceque bon Micha avait quand même super bien expliqué ^^
A chi stanta, à chi scurnochja. A chì stughji un perdi tempu .
-

ghjuvanotta - Carabin vétéran
- Messages: 362
- Inscription: 17 Sep 2008, 16:48
Re: la VSEPR
merci bcp je sais pas pourquoi je bloquais sur ca 
- ben83
- Carabin newbie
- Messages: 17
- Inscription: 22 Sep 2009, 15:17
9 messages
• Page 1 sur 1
Retourner vers Chimie générale
Qui est en ligne
Utilisateurs parcourant ce forum: Aucun utilisateur enregistré et 2 invités