Salut

!
Alors là... je t'avoue que tu as eu raison de te poser des questions, parce que l'illustration proposée par Guillaume n'est pas celle initialement voulue.
Pour faire claire, dans la molécule page 7 :
1) Il n'y a pas de carbanion.
2) Ce n'est pas une fonction carboxylique mais cétone.
Donc on va faire simple pour reprendre, j'ai suivi le texte explicatif, et la molécule devait sans doute être celle-ci :
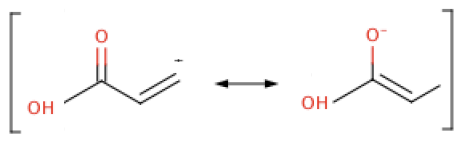
- mésomérie.png (8.71 Kio) Vu 550 fois
On a une mésomérie π - σ - π.
La fonction acide carboxylique est effet mésomère attracteur, donc elle va attiré la liaison pi du carbanion vers elle.
On remarque que la liaison pi est bien attiré vers l'acide carboxylique.
Il est bon de remarquer qu'il y a un respect des charges formelles.
Velcane a écrit: Dans les deux cas je ne vois pas pourquoi le O se retrouve avec une charge formelle (-).
La double liaison reliant l'oxygène au carbone se rompt (suite à la mésomérie) et monte vers l'oxygène, alors entouré de 3 dnl.
Pourquoi elle monte sur l'oxygène ?
Tout simplement parce que le carbone se doit de respecter la règle de l'octet ; et avec 2 doubles liaisons et 1 simple, il ne la respecte pas (10 électrons).
Voilà, je vais en parler à mon co-tut, il confirmera bien s'il y a une erreur de molécule dans la fiche, ou non (car c'est possible que je regarde la mauvaise illustration).
Bon courage

!

