Salut,
lulu24 a écrit:Qu'elle est la force ionique d'une solution aqueuse de 1 litre contenat 0,02 mole de NaCl et 0,01 mole de Na2SO4 ?
A 0,01
B 0,04
C 0,05
D 0,07
Il faut d'abord connaître la concentration de chaque ion dans cette solution de 1L:
- 0,02 mol de NaCl se dissocie en
0,02 mol de Na+ et
0,02 mol de Cl-.
- 0,01 mol de Na
2SO
4 se dissocie en
0,01 mol de SO42- et en
0,01 * 2 = 0,02 mol de Na+  C(Na+) = 0,02 + 0,02 = 0,04 mol/L
C(Na+) = 0,02 + 0,02 = 0,04 mol/L  C(Cl-) = 0,02 mol/L
C(Cl-) = 0,02 mol/L  C(SO42-) = 0,01 mol/L
C(SO42-) = 0,01 mol/Lµ = 0,5 *
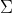
C
i * z
i2 avec z, l'électrovalence de l'ion (= le nombre de liaisons que peut faire l'ion)
 z(Na+) = 1
z(Na+) = 1 ;
z(SO42-) = 2 ;
z(Cl-) = 1µ = 0,5 * (
0,04 *
1² +
0,02 *
1² +
0,01 *
2²) = 0,5 * (
0,04 +
0,02 +
0,04) = 0,5 * 0,1 = 0,05 mol/L
lulu24 a écrit:À 1L de solution glucosé 5% on mélange 3g de KCl, exprimer en mol/kg la molalité de la solution finale?
A 0,33
B 0,47
C 0,28
D 0,15
E 0,04
On a 1L de solution glucosée à 5%

On a 5 g de glucose pour 0,1L de solution

On a donc 50 g de glucose dans la solution.
La masse de
SOLVANT est de 1 - 0,050 = 0,950 kg.
M(glucose) = 180 g/mol

n(glucose) = 50 / 180 = 0,28 mol
On ajoute à cette solution 3 g de KCl, de masse molaire M(KCl) = 75 g/mol

n(KCl) = 3 / 75 = 0,04 mol
La molalité de la solution finale est donc : C
m = (0,28 + 0,04) / 0,950 = 0,33 mol/kg
Voilà
 EDIT
EDIT : En relisant, je me suis aperçue qu'il y avait une petite coquille : j'ai donc remplacé "la masse de soluté" par "la masse de
SOLVANT"
 désoler de déranger mais je bloque sur 2 QCM
désoler de déranger mais je bloque sur 2 QCM 


