Salut à toi

C'est très simple cette histoire de nombres quantiques ! Tout d'abord qu'est ce que s'est ? Ils permettent en quelque sorte de discerner les différents électrons d'un atome, savoir où il se situent, et de représenter leur niveau d'énergie ! Puisque rappelons le, cette dernière est quantifiée !
- Le nombre quantique principal, c'est "n" ! Il détermine le niveau d'énergie dans lequel évolue ton electron, ce n peut prendre pour valeur 1 ( état fondamental ) jusqu'à l'infini ! n=1 correspondrait à la couche K, n=2 à la couche L ect... ( je fais appel à tes souvenirs de première ou terminale

)
--> Pour te le représenter mieux, y'a plusieurs paliers d'énergie dans lesquels se situent tes électrons, et ils sont de plus en plus rapprochés quand n augmente !
-Le nombre quantique secondaire est "l" ! Là ça correspondrait à des sous paliers, toujours quantifiés bien sur !
Ce nombre l est compris entre 0 et (n-1), c'est à dire si n=1, l=0 ! Si n=2, l=0 ou l=1 ! Et cette fois ça sert à décrire la forme de la zone de l'espace dans laquelle t'as une probabilité non nulle de trouver ton électron ! C'est ce qu'on appelle l'orbitale atomique (OA)

Illustration:

Et donc si l=0, ton orbitale est de type S ! Si l=1, elle est de type p, si l=2, de type d ! Enfin, si l=3, de type f, et t'iras pas plus loin en première année

!
-Le nombre quantique magnétique "m", lui représente encore un sous niveaux des paliers intermédiaires représentés par "l" ! Et m a une valeur comprise entre +l et -l

Ex: l=0, m= 0 Si l=1 , m=-1, 0, +1 ! C'est très simple, et en fait c'est autant de directions différentes dans l'espace pour ton orbitale atomique !
Par exemple, pour l=1, tu auras m compris entre -1 et +1, on est d'accord ? Donc il prendra pour valeur soit -1, 0, ou 1 ! Donc il y a 3 Orbitale atomique possibles pour l=1, les 3 OA seront dirigées dans trois directions différentes de l'espace qui ont la même énergie, on les dit juste dégénérées !
-Enfin le nombre quantique de spin "s", représente une propriété magnétique de l’électron, une rotation ! Le spin peut prendre deux valeurs opposées, soit un spin positif de +1/2 soit négatif de -1/2 ! Spin positif: ton électron représenté par une flèche est vers le haut dans la case quantique, spin négatif: il est vers le bas !
Illustration d'une case quantique avec des éléctrons:
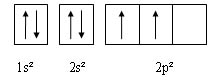
Voilà voilà, en espérant ne pas m'être trompé et avoir été assez clair

! Après si t'as d'autres questions nhésites pas






 ! C'est les mêmes OA, sauf qu'elles sont sur des paliers d’énergie différents ( d'où le 1 et le 2 devant s, qui représente le nombre quantique "n" ) !
! C'est les mêmes OA, sauf qu'elles sont sur des paliers d’énergie différents ( d'où le 1 et le 2 devant s, qui représente le nombre quantique "n" ) ! 

 ) mais plus abordable concernant les qcm que la thermo ou une erreur de calcul est souvent très vite arrivée et tu ne peux pas tout recommencer
) mais plus abordable concernant les qcm que la thermo ou une erreur de calcul est souvent très vite arrivée et tu ne peux pas tout recommencer