Je vais tenter de t'apporter quelques informations soldat Ups :soldier :
Donc comme tu le sais chaque élément possède un numéro atomique Z, correspondant au nombre de protons. De plus, le numero Z correspond au nombre d'électrons si ton élément n'est point ionisé. Suivant le nombre d'électron de notre élément X, on va remplir les case quantique en suivant les différentes règles que tu as du voir ( principe de Pauli, Hund etc ).
Justement concernant la loi de Hund, la valence secondaire est ce qu'on peut appeler ' une violation ' de la règle. Cependant elle reflète mieux la réalité pour des raisons de stabilités. On va prendre l'exemple du
Carbone avec un numero atomique
Z = 6 donc tu dois avoir comme répartition sur tes couches électroniques :
1s² 2s² 2p². Tu vois bien en répartissant tout ça sur des cases quantiques qu'on obtient une valence principale de 2 car il ne reste que 2 électrons célibataires au niveau de la
couche p. Cependant on assiste à un échange entre les sous-couches 2s et 2p comme ceci :
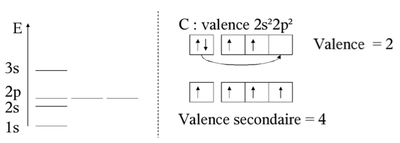
Cet échange te permet de passer de
2 à 4 électrons célibataires c'est donc ça qu'on appelle la valence secondaire,
c'est la dissociation de doublets non-liants par des échanges d'électrons entre orbite atomique s-p-d de même n, ici 2s et 2pVoilà, j'espère t'avoir aidé Ups, les tuteurs te répondront pour t'éclairer ! Shépard terminé !













