Par rapport à une mésomérie

Quand t'es à la base hybridé sp3 et que t'as une alternance, tu pourras délocaliser tes électrons
Mais ce sera pas n'importe quelle type de mésomérie, un DNL doit y être impliqué
Un exemple, la molécule d'imidazole:
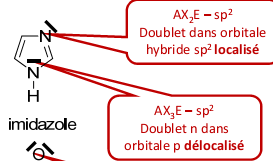
- Imidazole.png (11.57 Kio) Vu 199 fois
Azote du haut: Tu fais ta nomenclature VSEPR AXnEm, ton azote fait 3 liaisons ds 2 directions différentes et porte un DNL, il est AX2E1(c'est le nbr de directions, pas le nombre de liaisons qui compte pour X)
n+m=3, il est sp2. Ac sp2, t'auras pas de déloc
Azote du bas: L'azote fait 3 liaisons ds 3 directions différentes et porte un DNL, il est AX3E1
n+m=4, t'es sp3. Maintenant, tu regardes si t'as une mésomérie, si c'est le cas, tu délocalise, sinon, tu restes hybridé sp3
T'observes une mésomérie n-sima-pi, pour qu'elle ait lieu, ton doublet non liant doit être dans une orbitale p pure, hors, là il est dans une sp3. Du coup, tu vas baisser ton état d'hybridation et passer de sp3 à sp2 déloc.
C'est assez long mais c'est complet. C'est mieux





