Le Guide pour bien débuter la LAS : Ici
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Orbitales atomiques/orbitales moléculaires
20 messages
• Page 1 sur 1
Orbitales atomiques/orbitales moléculaires
BoNsOiR !
Quelqu'un pourrait m'expliquer pourquoi "à partir de 2 OA on crée 2 OM" ???
J'offre un twix
Quelqu'un pourrait m'expliquer pourquoi "à partir de 2 OA on crée 2 OM" ???
J'offre un twix
Dernière édition par Professeur Rogue le 21 Oct 2013, 13:46, édité 1 fois.
-

Professeur Rogue - Carabin vétéran
- Messages: 279
- Inscription: 07 Oct 2013, 17:39
Re: Orbitales atomiques/orbitales moléculaires
Gnafron, une réponse aussi rapide pour un twix ?! 
Plus sérieusement, l'autre sujet répond à ta question Rogue?

Plus sérieusement, l'autre sujet répond à ta question Rogue?
-

AhmedT - CM Forum
- Messages: 515
- Inscription: 23 Oct 2011, 15:15
Re: Orbitales atomiques/orbitales moléculaires
XD Ahmed ! Voui, ze veux mon twix maintenant ! 

-

Gnafron - Carabin vétéran
- Messages: 415
- Inscription: 07 Sep 2012, 12:01
Re: Orbitales atomiques/orbitales moléculaires
Bientôt le twix bientôt, parce que moi j'aurais plutôt dit qu'avec 2 OA on forme UNE OM, vu qu'on met en commun 2 e- non ?
-

Professeur Rogue - Carabin vétéran
- Messages: 279
- Inscription: 07 Oct 2013, 17:39
Re: Orbitales atomiques/orbitales moléculaires
Salut 
Le truc c'est qu'il n'y a pas que les électrons de liaison qui vont être sur les OM, il y a aussi les électrons de coeur...
Donc avec 2 OA, tu auras 4 électrons, donc forcément 2 OM
Bonne journée

Le truc c'est qu'il n'y a pas que les électrons de liaison qui vont être sur les OM, il y a aussi les électrons de coeur...
Donc avec 2 OA, tu auras 4 électrons, donc forcément 2 OM

Bonne journée

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: Orbitales atomiques/orbitales moléculaires
BoooOOooonnnNNNjour !!!
Je ne comprends point ton raisonnement... pourquoi les electrons de coeur jouent un role dans les liaisons ?
Et en plus pourquoi il y en aurait 4 ?
merci en tout cas
Je ne comprends point ton raisonnement... pourquoi les electrons de coeur jouent un role dans les liaisons ?
Et en plus pourquoi il y en aurait 4 ?
merci en tout cas

-

Professeur Rogue - Carabin vétéran
- Messages: 279
- Inscription: 07 Oct 2013, 17:39
Re: Orbitales atomiques/orbitales moléculaires
Non, les électrons de coeur ne jouent pas de rôle dans les liaisons.
Mais quand tu as la formation d'une molécule (avec 2 atomes), toutes les OA des 2 atomes se transforment en OM (je suis pas sur que ce soit au programme, c'est juste pour que tu comprennes )
)
Donc à partir de 2 OA (comprenant 2 e- chacune, donc 4 électrons au total), tu as la formation de 2 OM
Le prof prend un énorme raccourci sur la formation des OM (1 mois de cours en fac de science...) donc retiens juste que 2 OA donnent 2 OM
Mais quand tu as la formation d'une molécule (avec 2 atomes), toutes les OA des 2 atomes se transforment en OM (je suis pas sur que ce soit au programme, c'est juste pour que tu comprennes
 )
)Donc à partir de 2 OA (comprenant 2 e- chacune, donc 4 électrons au total), tu as la formation de 2 OM
Le prof prend un énorme raccourci sur la formation des OM (1 mois de cours en fac de science...) donc retiens juste que 2 OA donnent 2 OM

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: Orbitales atomiques/orbitales moléculaires
Je suis vraiment désolé, je ne comprend pas pourquoi tu dis que une orbitale atomique a 2 électrons, sinon ca ferait un doublet non liant et du coup pas de liaisons ...
En fait je pensais que cette phrase reprenais celle de la diapo juste en dessous qui dit que "2 OA peuvent donner 2 TYPES d'OM" et pas 2 OM,ce qui serait plus logique mais si la phrase du cours est bien vrai tel quel alors je comprend vraiment pas
Je suis désolé, si ça te fait perdre du temps ne t’embête pas j'attendrais la réponse d'un tuteur !
en tout cas merci pour tes explications
En fait je pensais que cette phrase reprenais celle de la diapo juste en dessous qui dit que "2 OA peuvent donner 2 TYPES d'OM" et pas 2 OM,ce qui serait plus logique mais si la phrase du cours est bien vrai tel quel alors je comprend vraiment pas
Je suis désolé, si ça te fait perdre du temps ne t’embête pas j'attendrais la réponse d'un tuteur !
en tout cas merci pour tes explications

-

Professeur Rogue - Carabin vétéran
- Messages: 279
- Inscription: 07 Oct 2013, 17:39
Re: Orbitales atomiques/orbitales moléculaires
Peut être que cette image t'aidera à comprendre (je l'ai prise du web) 
C'est une représentation des OM de la molécules d'O2 (les OM de type Sigma1s ne sont pas représentées)
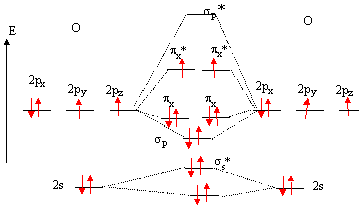

C'est une représentation des OM de la molécules d'O2 (les OM de type Sigma1s ne sont pas représentées)

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: Orbitales atomiques/orbitales moléculaires
Salut Rogue 
Voilà la diapo dont tu sembles parler
D'abord, les orbitales de cœur ne sont absolument pas au programme, elles n'ont pas d'influence sur les propriétés chimiques des molécules, donc oubliez les tout simplement
Sur cette diapo, on te dis qu'on peut former deux types d'OM, à savoir OM sigma et OM pi
Maintenant, quand tu lieras 2 atomes par une liaison simple, tu mélangeras 2 OA (chacune appartenant à un atome et portant un électron) et tu créeras 2 OM sigma. Une orbitale moléculaire sera anti-liante, elle sera haute en énergie et l'autre sera liante basse en énergie.
Les électrons auront ensuite tendance à se placer dans l'orbitale moléculaire basse en énergie, tout simplement pour stabiliser l'édifice, ton OM anti-liante sera donc vide, tes OM liante sera peuplée par les 2 e-, tu auras formation d'une liaison covalente.
Pour conclure, retiens que tu crées 2OM à partir de 2OA, et que tes électrons se placeront ds l'OM basse en énergie pour former ta liaison covalente
Ça t'éclaire, ça te va comme réponse?

Voilà la diapo dont tu sembles parler
D'abord, les orbitales de cœur ne sont absolument pas au programme, elles n'ont pas d'influence sur les propriétés chimiques des molécules, donc oubliez les tout simplement
Sur cette diapo, on te dis qu'on peut former deux types d'OM, à savoir OM sigma et OM pi
Maintenant, quand tu lieras 2 atomes par une liaison simple, tu mélangeras 2 OA (chacune appartenant à un atome et portant un électron) et tu créeras 2 OM sigma. Une orbitale moléculaire sera anti-liante, elle sera haute en énergie et l'autre sera liante basse en énergie.
Les électrons auront ensuite tendance à se placer dans l'orbitale moléculaire basse en énergie, tout simplement pour stabiliser l'édifice, ton OM anti-liante sera donc vide, tes OM liante sera peuplée par les 2 e-, tu auras formation d'une liaison covalente.
Pour conclure, retiens que tu crées 2OM à partir de 2OA, et que tes électrons se placeront ds l'OM basse en énergie pour former ta liaison covalente
Ça t'éclaire, ça te va comme réponse?
-

AhmedT - CM Forum
- Messages: 515
- Inscription: 23 Oct 2011, 15:15
Re: Orbitales atomiques/orbitales moléculaires
C'est splendide, c'est merveilleux j'ai tout compris merci AhmedT je te dois un twix en OR, et merci aussi Raboucho pour tes explications !!! 

-

Professeur Rogue - Carabin vétéran
- Messages: 279
- Inscription: 07 Oct 2013, 17:39
Re: Orbitales atomiques/orbitales moléculaires
ARGH j'ai raté le twix ! 

-

Gnafron - Carabin vétéran
- Messages: 415
- Inscription: 07 Sep 2012, 12:01
Re: Orbitales atomiques/orbitales moléculaires
De rien 
C'est vrai que je me suis un peu embrouillé dans les explications, et je me rappelais plus si les OM de coeur étaient au programme ou pas (et je pensais que c'était utile de comprendre pourquoi il y avait 2 OM )
)
Et du coup, j'ai pas le twix non plus ...

C'est vrai que je me suis un peu embrouillé dans les explications, et je me rappelais plus si les OM de coeur étaient au programme ou pas (et je pensais que c'était utile de comprendre pourquoi il y avait 2 OM
Et du coup, j'ai pas le twix non plus ...

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: Orbitales atomiques/orbitales moléculaires
juste j'ai envie de rajouter quelque chose parce que j'avais un peu du mal avec ça aussi , on a bien formation de 2 OM à partir de 2 OA seulement une seul sera peuplé ? ( la plus stable ) , et du coup celle qui est laisser vide c'est elle qui permet la formation de liaisons pi ou la mésomérie ? ( mais pour la mésomérie je suis pas sur étant donner que les 2 devaient se trouver dans des orbitales P ''pures" pour pouvoir se délocaliser ... )
-

Guillaume.M - Carabin Geek
- Messages: 734
- Inscription: 10 Oct 2012, 18:13
Re: Orbitales atomiques/orbitales moléculaires
Guillaume.M a écrit:on a bien formation de 2 OM à partir de 2 OA seulement une seul sera peuplé ? ( la plus stable )
Oui

Guillaume.M a écrit:et du coup celle qui est laisser vide c'est elle qui permet la formation de liaisons pi ou la mésomérie ? ( mais pour la mésomérie je suis pas sur étant donner que les 2 devaient se trouver dans des orbitales P ''pures" pour pouvoir se délocaliser ... )
Non, celle qui est laissée vide ne sert pas du tout pour les liaisons

A partir de 2 OA tu as formation de 2 OM, une liante et l'autre anti-liante. C'est deux OM sont soit sigma, soit pi. Donc tu auras soit sigma liant et anti-liant, soit pi liant et anti-liant
Les OM pi sont formés à partir d'OA p pures, donc pour la mésomérie, les e- sur les OM pi peuvent se délocaliser
C'est good ?
-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: Orbitales atomiques/orbitales moléculaires
ok mais qu'est ce qui différencie les OM sigma des pi ? ( recouvrement axial et latéral ? ) et du coup à partir d'OH on ne peut pas former d'OM pi ? et enfin , pourquoi les é on besoin d'étre dans une p " pure " pour pouvoir se délocaliser .. ( dsl bcp de questions mais je galère !!! )
-

Guillaume.M - Carabin Geek
- Messages: 734
- Inscription: 10 Oct 2012, 18:13
Re: Orbitales atomiques/orbitales moléculaires
ah et aussi les OM sigma anti liante ne servent à rien du coup ?
-

Guillaume.M - Carabin Geek
- Messages: 734
- Inscription: 10 Oct 2012, 18:13
Re: Orbitales atomiques/orbitales moléculaires
Guillaume.M a écrit:ok mais qu'est ce qui différencie les OM sigma des pi ? ( recouvrement axial et latéral ? )
C'est ça

Sigma : recouvrement axial
Pi : recouvrement latéral
Guillaume.M a écrit:et du coup à partir d'OH on ne peut pas former d'OM pi ?
Non, parce que sinon on ne peut pas avoir de recouvrement latéral
Guillaume.M a écrit:et enfin , pourquoi les é on besoin d'étre dans une p " pure " pour pouvoir se délocaliser ..
Je crois pas que ce soit au programme, mais ça doit être par rapport à la structure géométrique des OA p pures qui permettent un rapprochement entre elles pour la délocalisation des e- (je suis pas sur
 )
)Guillaume.M a écrit:( dsl bcp de questions mais je galère !!! )
tkt, les OA, OM et OH sont vu en 1 mois à la fac de science... je trouve que c'est un peu barbare de voir ça en 1 cours

Guillaume.M a écrit:ah et aussi les OM sigma anti liante ne servent à rien du coup ?
Pour les liaisons non, mais elles servent pour les OM de coeur (qui ne sont pas au programme)
Si tu veux un exemple, j'avais mis un schéma quelques post plus haut

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
20 messages
• Page 1 sur 1
Retourner vers Chimie Organique
Qui est en ligne
Utilisateurs parcourant ce forum: Aucun utilisateur enregistré et 1 invité





 N'oubliez pas de passer votre post en résolu svp
N'oubliez pas de passer votre post en résolu svp