
Le Guide pour bien débuter la LAS : Ici
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Barycentres
8 messages
• Page 1 sur 1
Barycentres
Coucou ! Alors est ce que quelqu un peut m expliquer comment reconnaît on une molécule polaire car je ne comprend pas comment on voit si les barycentres coïncident ou pas notamment dans le qcm 8 du DM ! Merci d avance 

Dernière édition par mariieyep le 22 Sep 2014, 17:58, édité 3 fois.
-

mariieyep - Carabin addicted
- Messages: 1621
- Inscription: 28 Mar 2013, 22:28
Re: Barycentres
Faut que tu fasses avec les delta + et - et tu regardes
Enfin jcrois
Enfin jcrois

- nissart2
- Carabin addicted
- Messages: 1050
- Inscription: 20 Sep 2013, 18:26
Re: Barycentres
Coucou,
Si les barycentres des charges + et - coincident ca veut dire que ta molecule est symétrique (dans le cas du dm les 2 longueurs sont pareilles) donc apolaire car les moments dipolaires s'annulent, si je dis pas de bêtises ^^
Si les barycentres des charges + et - coincident ca veut dire que ta molecule est symétrique (dans le cas du dm les 2 longueurs sont pareilles) donc apolaire car les moments dipolaires s'annulent, si je dis pas de bêtises ^^
Pour transformer un résultat faux en résultat juste, il suffit de lui ajouter une constante variable de même dimension adéquatement choisie que l'on nommera « constante de Murphy »
-

SonyaK - Carabin newbie
- Messages: 18
- Inscription: 08 Sep 2014, 14:33
Re: Barycentres
Salut ! 
La notion de polarité est une chose qui s'acquiert logiquement en comprenant les bases de chimie ne t'inquiète pas. Je te propose donc un début d'explication pour t'éclairer ça sera déjà très bien pour commencer !
Je te propose donc un début d'explication pour t'éclairer ça sera déjà très bien pour commencer !
Met au panier la notion de barycentre, c'est pas très pédagogique de ma part d'avoir foutu la déf du cours en guise d'explication mais je ne voyais pas quoi ajouter d'autre pour le coup car c'est presque intuitif le concept en fait.
Quand auras-tu une molécule apolaire ?
Dans le cas où les vecteurs allant d'une charge partielle - à une charge partielle + par convention s'annulent (si charges partielles il y a évidemment). C'est là qu'on dit que les barycentres "coïncident". Si ce n'est pas le cas, que de tels vecteurs ne s'annulent pas, ta molécule est polaire.
Prenons un exemple tout bête. La liaison C-H est légèrement polarisée en faveur du carbone plus électronégatif que l'hydrogène donc le carbone présente une charge partielle négative et l'hydrogène une charge partielle positive. Le carbone "pompe" le nuage électronique de l'atome d'hydrogène dont la charge positive du noyau n'est plus compensée totalement par l'électron qui gravite, attiré par le carbone.
Si on prend la molécule de méthane CH4, on aura 4 vecteurs allant de C vers H, chaque H présentant une charge partielle positive. Le C va se coltiner quatres charges partielles négatives car il attire l'électron de chacun des trois hydrogènes.
Or l'ensemble des vecteurs s'annulent (ils ont d'ailleurs la même longueur, s'écartant chacun les uns des autres d'un même angle) ceci donc grâce à la structure symétrique (tétraèdre) du méthane. La molécule n'a donc aucun pôle, elle est apolaire. Je sors paint.
Prenons l'eau H2O cette fois, c'est du cours. L'oxygène est bien plus électronégatif, et pompe le nuage électronique (donc l’unique électron) de chacun des deux hydrogène. Pourquoi la molécule est-elle polaire ? On va le voir en terme de vecteur. Souviens-toi, l'oxygène présente deux doublets non liants qui vont lui donner une forme dite coudée, qui repoussent les liaisons faites avec les hydrogènes.
Voilà, ces deux exemples devraient te suffire je pense.
Désormais tu vas trouver le QCM très simple vu que c'est tout en 2D.
Pour la molécule (1), les vecteurs s'annulent c'est nickel la molécule apolaire.
Pour la molécule (2), non un des vecteurs est plus long et ne s'annule pas avec l'autre, la molécule est polaire.
N'hésite pas si tu as d'autres question ou si tu veux une précision, bon courage pour mardi.

La notion de polarité est une chose qui s'acquiert logiquement en comprenant les bases de chimie ne t'inquiète pas.
 Je te propose donc un début d'explication pour t'éclairer ça sera déjà très bien pour commencer !
Je te propose donc un début d'explication pour t'éclairer ça sera déjà très bien pour commencer !Met au panier la notion de barycentre, c'est pas très pédagogique de ma part d'avoir foutu la déf du cours en guise d'explication mais je ne voyais pas quoi ajouter d'autre pour le coup car c'est presque intuitif le concept en fait.
Quand auras-tu une molécule apolaire ?
Dans le cas où les vecteurs allant d'une charge partielle - à une charge partielle + par convention s'annulent (si charges partielles il y a évidemment). C'est là qu'on dit que les barycentres "coïncident". Si ce n'est pas le cas, que de tels vecteurs ne s'annulent pas, ta molécule est polaire.
Prenons un exemple tout bête. La liaison C-H est légèrement polarisée en faveur du carbone plus électronégatif que l'hydrogène donc le carbone présente une charge partielle négative et l'hydrogène une charge partielle positive. Le carbone "pompe" le nuage électronique de l'atome d'hydrogène dont la charge positive du noyau n'est plus compensée totalement par l'électron qui gravite, attiré par le carbone.
Si on prend la molécule de méthane CH4, on aura 4 vecteurs allant de C vers H, chaque H présentant une charge partielle positive. Le C va se coltiner quatres charges partielles négatives car il attire l'électron de chacun des trois hydrogènes.
Or l'ensemble des vecteurs s'annulent (ils ont d'ailleurs la même longueur, s'écartant chacun les uns des autres d'un même angle) ceci donc grâce à la structure symétrique (tétraèdre) du méthane. La molécule n'a donc aucun pôle, elle est apolaire. Je sors paint.
Prenons l'eau H2O cette fois, c'est du cours. L'oxygène est bien plus électronégatif, et pompe le nuage électronique (donc l’unique électron) de chacun des deux hydrogène. Pourquoi la molécule est-elle polaire ? On va le voir en terme de vecteur. Souviens-toi, l'oxygène présente deux doublets non liants qui vont lui donner une forme dite coudée, qui repoussent les liaisons faites avec les hydrogènes.
Voilà, ces deux exemples devraient te suffire je pense.

Désormais tu vas trouver le QCM très simple vu que c'est tout en 2D.
Pour la molécule (1), les vecteurs s'annulent c'est nickel la molécule apolaire.
Pour la molécule (2), non un des vecteurs est plus long et ne s'annule pas avec l'autre, la molécule est polaire.
N'hésite pas si tu as d'autres question ou si tu veux une précision, bon courage pour mardi.

- Mewtwo
- Tut' Biophy/Physique

- Messages: 766
- Inscription: 20 Oct 2013, 18:53
- Localisation: Caverne azurée
Re: Barycentres
Merci beaucoup d avoir pris le temps de me faire une super explication détaillée c est très gentil !! Je comprends le qcm 8 et j espère que je ne me tromperai plus sinon je t embêterai encore un peu 

-

mariieyep - Carabin addicted
- Messages: 1621
- Inscription: 28 Mar 2013, 22:28
Re: Barycentres
Euh juste c'est pas 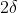 - sur O et
- sur O et 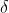 + sur chaque H ? ^^
+ sur chaque H ? ^^
- nissart2
- Carabin addicted
- Messages: 1050
- Inscription: 20 Sep 2013, 18:26
Re: Barycentres
Oui bien sûr Nissart ^^ Quel étourdi je fais.
Par contre la prochaine fois si ça a un quelconque rapport avec le DM il faut le préciser dans le titre, merci.
Par contre la prochaine fois si ça a un quelconque rapport avec le DM il faut le préciser dans le titre, merci.
- Mewtwo
- Tut' Biophy/Physique

- Messages: 766
- Inscription: 20 Oct 2013, 18:53
- Localisation: Caverne azurée
Re: Barycentres
Oui pardon et encore merci 

-

mariieyep - Carabin addicted
- Messages: 1621
- Inscription: 28 Mar 2013, 22:28
8 messages
• Page 1 sur 1
Qui est en ligne
Utilisateurs parcourant ce forum: Aucun utilisateur enregistré et 2 invités
