Coucou,

Déjà, désolée de répondre si tard!
Alors pour faire ce genre de cycle thermo il faut tout d'abord que tu comprènes bien ce qu'on te demande de trouver, ici c'est l'énergie de la liaison O-H de la molécule d'H20 (H20 a donc 2 liaisons OH). Après, dans un deuxième temps tu regardes tes données et t'essayes de trouver un moyen de les utiliser.
On te donne ∆
fH
0 (H
2O
(l)), or tu sais que lorsque qu'on parle d'enthalpie standard de formation d'une molécule, les espèces doivent être dans leur
état standard de référence (à savoir H
2(g) et O
2(g)).
 H2(g) + 1/2 O2(g) --> H20 (l)
H2(g) + 1/2 O2(g) --> H20 (l) Je vais utiliser cette réaction comme réaction "principale" pour déterminer le sens de mes flèches. Il faut que les flèches des étapes intermédiaires aillent dans le même sens que la réaction princpiale.
Tu mets
1/2 O2 parce que tu n'as qu'un seul atome d'oxygène dans ta molécule d'H
2O
Tu sais que pour former tes liaisons O-H tu vas avoir besoin de briser tes liaisons O-O et H-H pour qu'ils soient sous forme d'atomes simples. (rappel: on brise des liaisons, énergie comptée positivement)
Ensuite tu formes tes liaisons O-H (énergie comptée négativement) pour former ta molécule d'H2O, ces énergie de liaison sont tes inconnues (je les ai notées
x), c'est ce que tu cherches à calculer. Une fois formée, elle est sous forme gazeuse car on part d'atome sous forme gazeuse et car
l’énergie de liaison d’une molécule diatomique AB, notée DA-B , est la variation d’énergie interne standard de la réaction de dissociation d’une mole de AB gazeux, à 0 K, en deux radicaux A et B gazeux.Maintenant tu construis ton cycle thermo :
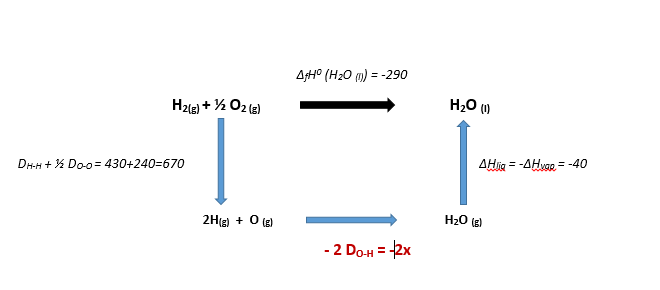
- Cyclethermoex9livre.PNG (6.91 Kio) Vu 441 fois
Il te reste plus qu'a tout additionner en utilisant la loi de Hess.
Tu te retrouves donc avec :
∆
fH
0 (H
2O
(l)) = DH-H + ½ DO-O - 2 DO-H -∆Hvap H2O(l)
-290 = 430+240-2x-40
-290 = 630-2x
2x = 920
x = 460
L'énergie de la liaison H-O vaut donc 460 kJ.mol-1
(vous noterez une petite erreur dans le livre du prof...)J'espere que c'est plus clair pour toi, bon courage pour demain



 :
:



 :
:







