Re bonsoir,
Alors dans le 1er qcm que tu as donné (noté QCM 6),
Le plus dur ici, était de savoir que dans son état de référence on note le silicium à l'état solide de cette façon : Si
(s) Ensuite il fallait reproduire le cycle permettant d'aboutir à la molécule SiO
2(s) tel quel :
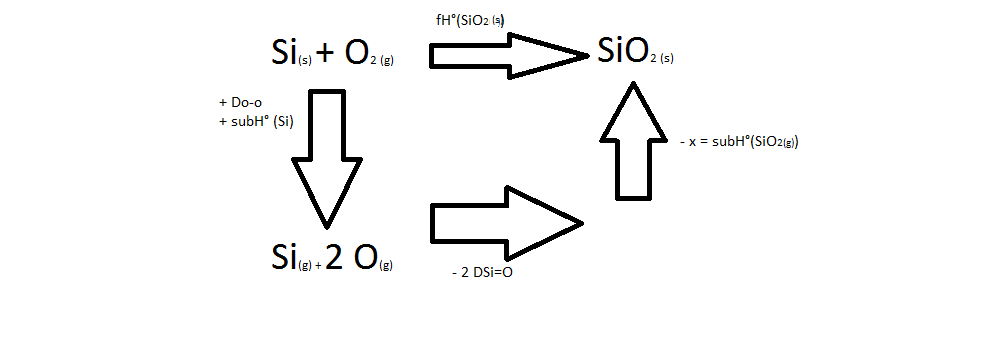
- qcmreponse.png (9.16 Kio) Vu 299 fois
A partir de là, on peut calculer l'enthalpie de sublimation de la molécule SiO
2(s) Soit : fH°(SiO
2(s) ) = Do-o + subH°(Si) - 2DSi=O - subH°SiO
2(g) -911 = 498 + 399 - 2 x 796 - x
x = 911 + 498 + 399 - 1592
x = 216 kJ.mol
-1Ça va mieux ?

___________________________
Pour le 2ème QCM (QCM 4 sur ta fiche) on fait ce cycle là grâce aux données de l'énoncé ; comme tu peux le constater on part des états standard de l'eau donc H
2(g) et 1/2 O
2(g) parce qu'on a besoin d'un seul atome d'oxygène
Ensuite grâce aux données : enthalpie de formation de l'eau gazeuse on forme de la gazeuse et on utilise l'opposé de l'enthalpie de vaporisation car on nous demande un produit liquide à partir d'un produit gazeux
Je le rappelle :
liquide -> gazeux = vaporisation /
gazeux -> liquide = liquéfaction
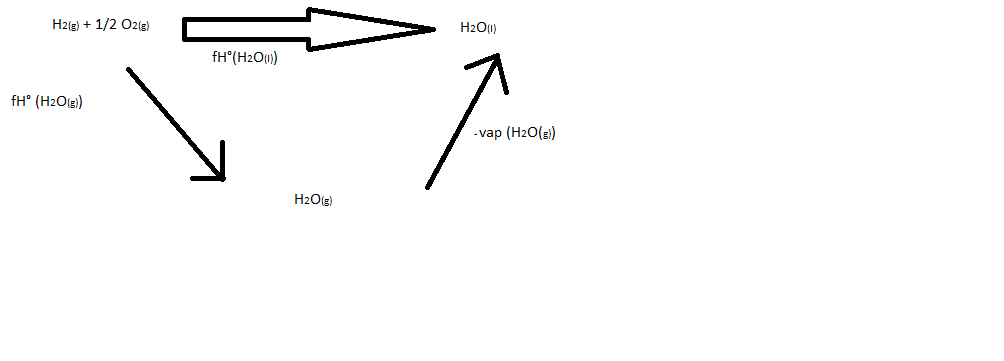
- qcmreponse2.png (6.4 Kio) Vu 299 fois
Donc fH°(H
2O
(l)) = fH°(H
2O
(g)) - vapH°(H
2O
(g))
fH°(H
2O
(l)) = - 242 - 43
fH°(H
2O
(l)) = - 285 kJ.mol
-1Est-ce que c'est un peu plus clair ?












 )
)