Salut

L'hybridation d'un
atome va lui permettre de
mélanger ses orbitales atomiques s et p d'énergie différente pour former des
orbitales hybrides sp de
même énergie et de même longueur. Cela a un impact sur la
géométrie de la molécule. En effet, un atome hybridé sp3 aura une conformation tétraédrique, un atome hybridé sp2 une conformation trigonale plane et celui hybridé sp une conformation linéaire.
Ex : NH3 (l'ammoniac)
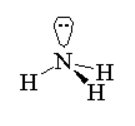
- ammoniac.png (3.19 Kio) Vu 546 fois
On a ici AX
3E cad 4 directions différentes
On va donc vouloir former
4 orbitales hybrides sp pour pouvoir former
4 liaisons σ identiques et aboutir à une
géométrie tétraèdrique (cad 4 directions).
L'hybridation des orbitales atomiques s et p de l'azote permet d'expliquer que les
liaisons σ soient identiques en énergie et en taille. Ce ne serait pas le cas si certaines de ces liaisons étaient formées par une orbitale atomique 2s et d'autres par des OA 2p !
Dans l'exemple de l'ammoniac, l"azote est hybridé sp
3 (=mélange d'1 orbitale s + 3 orbitales p = 4 liaisons identiques).
Ce qu'il faut retenir : 
L'hybridation permet d'avoir des liaisons de même énergie.

L' atome change
d'état d'hybridation selon la
géométrie demandée par la
molécule qu'il forme (cf : AXnEm) (
ex : le C du méthane (CH4) est hybridé
sp3 (4 directions

4 OH), le C de l'éthène (CH2=CH2) est hybridé
sp2 (3 directions

3 OH))

L'atome peut aussi changer son hybridation en
délocalisant un e- à cause d'une
mésomérie.
Dans le cadre d'un dnl, cela est possible uniquement si au départ, on avait une hybridation de type
sp3. En effet, pour être
délocalisé, l'e- doit être contenu dans une
orbitale p pure ou π et participer à une mésomérie. Pour un atome doté d'un dnl, on va donc passer d'une
hybridation sp3 (4 OH) à une hybridation
sp2 déloc (cad
3 OH + 1 OA p pure).
C'est bon pour toi ?

Bonne journée











 C'est qd même plus clair d'un coup ! Merci bcp
C'est qd même plus clair d'un coup ! Merci bcp