Coucou!

Merci c'est super gentil! C'est sympa d'avoir des retours positifs!

Alors enfaite ton H2SO4 se scinde en H2O et en HSO3.

Bon déjà, le H2SO4 se décompose en H+ et HSO4-.
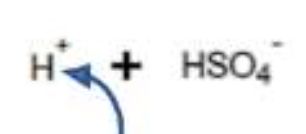
- Capture d’écran 2021-02-21 à 14.36.52.png (29.9 Kio) Vu 316 fois

La on a une déprotonation, du coup, le H+ peut aller se fixer sur un des DNL d'un des oxygènes du HSO4- et donner OH et HS03.
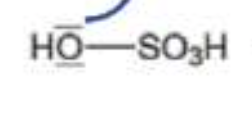
- Capture d’écran 2021-02-21 à 14.35.59.png (25.25 Kio) Vu 316 fois

Du coup ton OH possède 2 DNL, un autre H peut venir se fixer sur l'oxygène et donner H2O. Ici on veut remettre les charges neutres sur l'oxygène, donc la double liaison va se rabattre sur l'oxygène qui va être attirée par les charges négatives, et ça va donc casser la liaison et donc donner H2O et HS03.
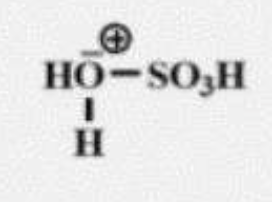
- Capture d’écran 2021-02-21 à 14.39.41.png (57.34 Kio) Vu 316 fois

Et donc notre espèce électrophone HSO3 va venir se fixer le cycle aromatique, don ici le benzène.
Dis moi si tu as compris, sinon j'essayerais de t'expliquer autrement!
Bonne chance pour la suite, et continues de bosser à fond l'UE15!
Si tu as des questions par rapport à la Pharma, Marseille ou quoi que ce soit, n'hésite pas

Bisous


 ) et dans la partie sur les substitutions électrophiles je comprend pas trop comment se déroule le mécanisme de sulfonation, en fait c'est surtout la formation de l'électrophile dont je comprend pas le déroulement.
) et dans la partie sur les substitutions électrophiles je comprend pas trop comment se déroule le mécanisme de sulfonation, en fait c'est surtout la formation de l'électrophile dont je comprend pas le déroulement. 





