Kikou !
1. Il faut comprendre que c'est le groupement C=O (qui est soit une cétone, soit une aldéhyde)
ne peut pas faire d'effet mésomère tout seul comme un grand. Donc, il faut le rattacher à une molécule. Exemple du prof :
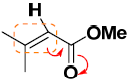
Il faut tout de suite comprendre que ce n'est pas forcèment une délocalisation n-sigma-pi. Ici, en l'occurence, on a pi-sigma-pi.
Tu vois bien que la cétone, ici, va choper la double liaison pour elle. Elle va attirer la double liaison. (Bon, j'avoue, que c'est grossièrement dit, le principe, c'est la compréhension). Donc, le groupe C=O est bel est bien mésomère attracteur et appauvrit la double liaison.
2.
plus l'énergie est basse, plus l'édifice est stable.
Prenons comme exemple les conformères décalés anti/gauche, ils sont plus stables que les conformations éclipsés/syn, donc de plus faible énergie.
Par la chimie G, on sait que
les orbitales s sont remplies avant les orbitales p. Donc, la couche s est plus proche du noyau de l'atome que la couche p, qui elle est par conséquent plus périphérique.
Qui possèdent l'énergie la plus faible ? Les electrons proches du noyau.
--> On en déduit facilement que les électrons de la couche p partent avant la couche s.
3. N=7 : 1s2, 2s2, 2p3. Etat basale : NH3-.
Si un hydrogène chargé positivement (H+) vient faire coucou à ton NH3-. Une liaison ionique va se créer entre le dnl du NH3- et la case vacante de l'hydrogène --> NH4+.
Pourquoi on met une charge positive ? Tout simplement parce que l'atome d'azote a perdu un électron. Il a du en céder un à l'hydrogène.
MAIS, ton azote respecte quand même la règle de l'octet (s'explique par la valence secondaire de l'atome d'azote de la molécule NH4+), alors de mettre une case vacante sur l'atome d'azote est FAUX !
4. L'atome d'azote a une théorie VSEPR de AX2E (ne pas oublié l'H) ==> hybridé sp2. Un hétéroatome hybridé sp2 voit son dnl localisé dans une orbitale hybridé p. Son dnl ne peut plus bouger, il est comme coincé. Pour que le dnl puisse voyager, il faut que l'azote soit hybridé sp3
obligatoirement.
Voili

.
A + !


