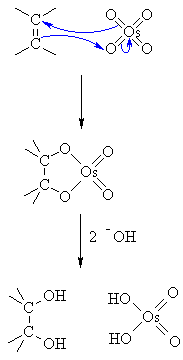
J'ai des questions sur cette partie que je ne comprend pas trop
1) je ne comprend pas du tout le mécanisme avec Oso4/ZhHcl/KMno4 (première réaction de la derniere page de la ronéo 6) Normalement je procède comme ça : je recopie ce qui change pas puis je fais l'attaque avec ce qu'on nous propose, la je vois pas ce qui change pas et je comprend pas comment on sait dans quel plan attaquer
EDIT : je crois avoir compris -> on attaque dans le même plan (avec les OH du même cote) et le reste je le met dans deux plans opposes
2) comment différencier la 1ère réaction de la deuxième ? En gros comment je sais laquelle il faut faire ? (je sais que ça aboutit a plusieurs produits mais bon..)
3) "le mécanisme n'est pas a connaitre ici, seul le bilan des réactions est a connaitre " euh, donc pour moi j'ai bien compris qu'on coupait au milieu de la liaison pi et qu'on rajoutait un O c'est tout ce qu'il faut savoir ?
4) toutes ces réactions sont bien stéréospécifiques ET stereoselectives ? Et regioselective..?
Et c'est tout
 merci !!
merci !!