Hello

Alors en fait il n'y pas d'erreur, quand la résine est
anionique, elle est
chargée -, donc elle attire les cations, qu'elle va échanger contre des H+ (d'où le nom d'
hydrogénée pour cette résine)
Quand elle est
cationique, elle est
chargée +, elle attire les anions, qu'elle échange contre les OH- (donc résine
hydroxylée)
Au final, puisqu'on a autant de cations que d'anions (car toute solution est normalement neutre), on produit autant d'ions H+ que d'OH-, qui par la réaction :
H
+ + OH
- = H
2O
vont tous se recombiner en eau (du fait que la constante d'équilibre de cette réaction dans ce sens est vraiment très faible, genre 10
-14).
Au final, il te restera peut-être 10-7 d'ions H+ et OH-, mais c'est normal du fait de cette réaction qui peut se produire dans les 2 sens, et tu obtiens bien l
'eau déminéralisée par la bipermutation.
Donc pour visualiser en schéma ça se passe comme ça :
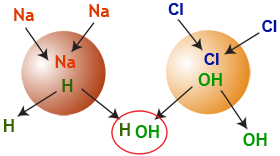
- demin.png (20.76 Kio) Vu 405 fois
Avec à droite la résine cationique (hydroxylée) et à gauche la résine anionique (hydrogénée) et au final tout se retransforme en eau !
Et pour ta question de pH, tout est dans la même solution, ça se recombine et les ions H+ et OH- restant sont en même nombre (à peu près, on va pas chipoter

) donc pH=7 !
C'est mieux comme ça

?


 ) donc pH=7 !
) donc pH=7 ! !
!