Salut

Il faut pour résoudre cet exercice utiliser la formule de la force ionique :
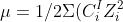)
.
Il faut donc pour commencer calculer l'ionarité lié à chacun des ions


Pour le K+, on ajoute 1 L à 0,3 mol/L, on ajoute donc 0,3 mol de KCl.
On a donc une concentration molaire de 0,3/3=0,1 mol/L au final

On multiplie par le nombre d'ions K+ formés et ça fait 1*0,1=0,1 mol d'ions/L


Pour le Ca2+, on ajoute 2 L à 0,1 mol/L, on ajoute donc 0,2 mol de CaCl2.
On a donc une concentration molaire de 0,2/3=0,067 mol/L au final

On multiplie par le nombre d'ions Ca+ formés et ça fait 1*0,067=0,067 mol d'ions/L


Pour le Cl-, c'est plus compliqué. On ajoute 1L à 0,3 mol/L donc 0,3 mol d'une part. Ce qui fait 0,3/3=0,1 mol/L venant du KCl, ce qui donne en ionarité 0,1*1=0,1 mol d'ions/L puisqu'on forme un seul ion Cl-

D'autre part, on ajoute 2 L à 0,1 mol/L. On a alors 0,2 mol apportées, ce qui fait 0,067 mol/L venant du CaCl2. En ionarité, on trouve 0,067*2=0,13 mol d'ions/L car on forme 2 Cl- à partir d'un CaCl2

Soit une ionarité totale de 0,1+0,13=0,23 mol d'ions/L oour le Cl-

Maintenant on peut calculer la force ionique :
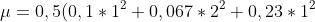=0,5*(0,1+0,27+0,23)=0,5*(0,1+0,5)=0,5*0,6=0,3 mol/L)
, on est bons

Bonne journée !
 Je comprends pas ce QCM si quelqu'un peut me l'expliquer avec une correction détaillé ce serait top !!
Je comprends pas ce QCM si quelqu'un peut me l'expliquer avec une correction détaillé ce serait top !! 




