Re
Voilà la base, ça c'est ce que tu conçois si j'ai bien compris

si n+m = 2 : sp

si n+m = 3 : sp
2 
si n+m = 4 : sp
3Maintenant, quand il ya mésomérie, c'est plus aussi simple.
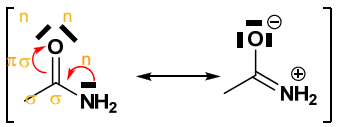
- méso.png (6.72 Kio) Vu 224 fois
Ici il y a mésomérie n-sigma-pi. Quand t'as une mésomérie, tu vas baisser l'état d'hybridation de sp3 à sp2, pour que le doublet soit dans une orbitale p pure. Ton azote sera dit sp2 délocalisé.
Des exemples:
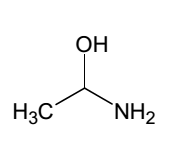
- sp3.png (2.92 Kio) Vu 224 fois
Ici pas de mésomérie, ton azote est AX3E, on a une hybridation sp3
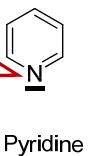
- Pyridine.png (2.91 Kio) Vu 224 fois
La pyridine a un azote hybridé sp2. Le DNL sera localisé, il ne participera pas à la mésomérie. Par contre on aura ici d'une part une orbitale p pure qui participe à la double liaison avec l'atome de carbone, d'autre part une mésomérie pi-sigma-pi
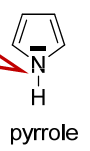
- Pyrrole.png (3.22 Kio) Vu 224 fois
L'azote du pyrrole est hybridé sp2 déloc. Il y a mésomérie n-sigma-pi, ton doublet non liant va se délocaliser, tu vas baisser ton état d'hybridation et passer de sp3 à sp2 déloc.
C'est mieux?




