Salut

Un doublet d'électron peut être représenté
soit par un doublet non liant, soit par une liaison.
- N3-.png (11.85 Kio) Vu 216 fois
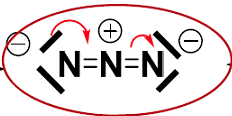
Pour le N3-, effectivement, chaque N a une valence de 5, tu rajoutes un électron dû à la charge, ça te fait 16e-, donc 8 doublets d'électrons.
Tu place tes 3 N, tu commences par les lier, puis tu mets tes DNL, tes 8 doublets sont placés
- (SO4)2-.png (3.79 Kio) Vu 216 fois
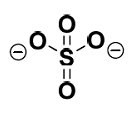
Pour le (SO4)2-, chaque atome a une valence de 6, et tu rajoutes 2 électrons dus aux charges formelles pour un totale de 32 électrons, soit 16 doublets
(ton compte est bon)Tu places ton souffre au milieu, tu le mets en hypervalence lui permettant de faire 6 liaisons, que tu fais avec tes 4 atomes d'oxygène, il nous reste 10 doublets à placer.
Ces doublets, comme tu ne peux plus faire de liaisons supplémentaires, seront placés sur les Oxygènes en tant que doublets non liants
(non représenté ici, c'est ça je pense qui t'a destabilisé). 3 doublets non liants seront placés sur les O portant une charge - ( donc ne liant le souffre qu'une fois) et 2 sur les O sans charges liant le souffre 2 fois
C'est mieux?
Désolé du temps de réponse 
 concernant la structure mésomère limite je ne suis pas sur d'avoir très bien compris comment on distribue les doublets d'electrons sur les molécules. Pour le N3- on compte les electrons de valence soit 15e + 1 car il y a la charge - donc 16 = 8 doublets. En bas de la page pour le SO4,2- je compte 4 oxygene de 6e de valence + 6e de valence pour le souffre ce qui nous donne 30 e de valence + 2e ( car 2-) donc 32 = 16 doublets d'e- mais je n'en vois que 7. Est ce que je suis a cote de la plaque ? Ou c'est une erreur peut etre ? Merci
concernant la structure mésomère limite je ne suis pas sur d'avoir très bien compris comment on distribue les doublets d'electrons sur les molécules. Pour le N3- on compte les electrons de valence soit 15e + 1 car il y a la charge - donc 16 = 8 doublets. En bas de la page pour le SO4,2- je compte 4 oxygene de 6e de valence + 6e de valence pour le souffre ce qui nous donne 30 e de valence + 2e ( car 2-) donc 32 = 16 doublets d'e- mais je n'en vois que 7. Est ce que je suis a cote de la plaque ? Ou c'est une erreur peut etre ? Merci  )
)







 N'oubliez pas de passer votre post en résolu svp
N'oubliez pas de passer votre post en résolu svp 