Yo,
Les réactions au sens Bronsted sont une particularité des réactions Lewis
Lewis: Quasi pas vu en P1, c'est l'attaque d'une case vacante par un DNL
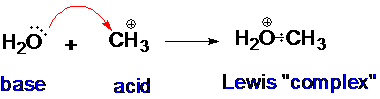
- Réaction Lewis.gif (2.29 Kio) Vu 184 fois
Bronsted: Celles étudiées en P1.C'est l'attaque d'un proton H+ par un DNL
Ici, un H+ s'en ira de la molécule d'eau et se fera attaquer par le DNL
Ensuite, oui, toute base sera nucléophile. Pk? Parce que ce sont des espèces en excès d'électrons qui chercheront à les partager ac des espèces électrophiles chargées + formellement ou partiellement
Cependant, rien ne dis que ts ces nucléophiles seront de bons nucléophiles, l'encombrement est un facteur important de baisse de cette nucléophilie
MC SCHURROS a écrit:Other question too ^^ : dans l'électronégativité, ça marche sur les liaisons pi ^^ ?
viewtopic.php?f=481&t=38739&p=247086&hilit=%C3%A9lectron%C3%A9gativit%C3%A9#p247086 
Non, par sur les pi, seulement les sigma. Cpdt les liaisons double/triple sont composé d'une sigma, tu px dc logiquement observé cet effet, mais ils ne représentent rien face aux effets mésomères svt présents lors de la présence d'une double liaison
Je te conseille de ne pas te prendre la tête ac cette question
 ,
,

