Salut Oxo
Alors sache que c'est sur ça que repose TOUUT le principe de séquençage de l'ADN via la méthode SANGER. Donc c'est absolument primordiale que tu visualises et que tu comprennes cela

Mais ne t'inquiètes pas, on va tout reprendre et ce sera touuut limpide je l'espère

 Tu as ton ADN dont tu veux connaître la séquence. Bon on parle pas du génome complet avec la méthode sanger car c'est trop long trop fastidieux (cf séquenceur à haut débit ou NGS, je t'invite à regarder le bonus des diapos de la tut rentrée super complète à ce sujet ). La méthode dite de Sanger est assez ciblée sur un gène que l'on connait déjà (du coup on a les amorces spécifiques ect), et sur lequel on veut voir si il y a une ou des mutations.
Tu as ton ADN dont tu veux connaître la séquence. Bon on parle pas du génome complet avec la méthode sanger car c'est trop long trop fastidieux (cf séquenceur à haut débit ou NGS, je t'invite à regarder le bonus des diapos de la tut rentrée super complète à ce sujet ). La méthode dite de Sanger est assez ciblée sur un gène que l'on connait déjà (du coup on a les amorces spécifiques ect), et sur lequel on veut voir si il y a une ou des mutations.
 premièrement on va amplifier spécifiquement la région d'ADN qui nous intéresse par PCR (dénaturation 90°/hybridation amorces 55°/élongation 72°). Ce sera plus pratique pour travailler sur plein de produit PCR que sur un fragment de KRS nanoscopique... jusque là logique
premièrement on va amplifier spécifiquement la région d'ADN qui nous intéresse par PCR (dénaturation 90°/hybridation amorces 55°/élongation 72°). Ce sera plus pratique pour travailler sur plein de produit PCR que sur un fragment de KRS nanoscopique... jusque là logique
 on passe maintenant au séquençage qui reprend les principes de base de la PCR : dénaturation / hybridation / élongation, à la différence près que :
on passe maintenant au séquençage qui reprend les principes de base de la PCR : dénaturation / hybridation / élongation, à la différence près que :
- la polymérase utilisée n'est pas la Taq et fonctionne alors à 60 ° et non 72 ° comme la TaqPol
- on a besoin que d'un seul primer car on veut seulement connaître la séquence du brin codant ( qui contient l'information =/= du brin non codant qui sert de matrice à la transcription souvenir biomol  ) C'est pas dit dans le cours, mais tu prendrais un primer complémentaire du brin codant ou non codant, pour accéder directement à la séquence du gène ? On voit ça à la fin ...
) C'est pas dit dans le cours, mais tu prendrais un primer complémentaire du brin codant ou non codant, pour accéder directement à la séquence du gène ? On voit ça à la fin ...
- on utilise en plus des dntps, des ddntps qui on la particularité de bloquer l'élongation quand ils sont insérés et d'être fluorescent avec une couleur spécifique à chaque nucléotides ATGC.
 Voilà pour les différences majeurs, maintenant c'est très simple la polymérase va synthétiser le brin fils = l'élongation. Et de manière totalement aléatoires elles va intégrer des ddntps ; en position 532 par exemple, ce qui va bloquer l'élongation à ce niveau. On a plein d'ADN car on a effectué une PCR préalablement, donc chaque "ADN parent" lors de l'étape d'élongation va intégrer un ddntp à un endroit différent.
Voilà pour les différences majeurs, maintenant c'est très simple la polymérase va synthétiser le brin fils = l'élongation. Et de manière totalement aléatoires elles va intégrer des ddntps ; en position 532 par exemple, ce qui va bloquer l'élongation à ce niveau. On a plein d'ADN car on a effectué une PCR préalablement, donc chaque "ADN parent" lors de l'étape d'élongation va intégrer un ddntp à un endroit différent.
 Du coup au final, tu auras toutes les tailles de fragments d'ADN avec en dernière position un ddntp (qui a bloqué l'élongation). Et on est capable de dire qu'elle est la nature de ce ddntp ATG ou C en fonction de la couleur du fluorochrome associé au ddntp.
Du coup au final, tu auras toutes les tailles de fragments d'ADN avec en dernière position un ddntp (qui a bloqué l'élongation). Et on est capable de dire qu'elle est la nature de ce ddntp ATG ou C en fonction de la couleur du fluorochrome associé au ddntp.
 Mais avant il faut séparer les fragments par taille pour pouvoir lire quelque chose. On utilise un séquenceur capillaire et dans ce capillaire un peu avec le même principe que l'électrophorèse tu vas avoir les fragments les plus légers qui vont migrer loin et inversement.
Mais avant il faut séparer les fragments par taille pour pouvoir lire quelque chose. On utilise un séquenceur capillaire et dans ce capillaire un peu avec le même principe que l'électrophorèse tu vas avoir les fragments les plus légers qui vont migrer loin et inversement.
 Les fragments les plus légers sont ceux qui ont inséré un ddntp tôt dans leur séquence, donc ce sont les premiers nucléotides dans la séquence de notre gène d'intérêt. Et à contrario, les fragments les plus lourd sont ceux qui ont intégrés un ddntp tardivement dans leur séquence, donc ce sont les derniers nucléotides de la séquence qu'on essaye de lire à la recherche d'une mutation
Les fragments les plus légers sont ceux qui ont inséré un ddntp tôt dans leur séquence, donc ce sont les premiers nucléotides dans la séquence de notre gène d'intérêt. Et à contrario, les fragments les plus lourd sont ceux qui ont intégrés un ddntp tardivement dans leur séquence, donc ce sont les derniers nucléotides de la séquence qu'on essaye de lire à la recherche d'une mutation 
 Une caméra laser lit la fluorescence, ça fait un pic à l'écran (rouge, vert, bleu ou jaune) et déchiffre la séquence du gène, par exemle : vert = Adénine, bleu = guanine ect
Une caméra laser lit la fluorescence, ça fait un pic à l'écran (rouge, vert, bleu ou jaune) et déchiffre la séquence du gène, par exemle : vert = Adénine, bleu = guanine ect
 Voilà on a séquencé notre ADN par PCR-séquençage (ici avec l'exemple du séquenceur capillaire).
Voilà on a séquencé notre ADN par PCR-séquençage (ici avec l'exemple du séquenceur capillaire).Voilà ce que ça donne :
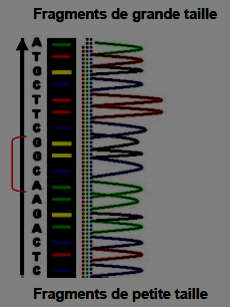
- Image2.png (69.78 Kio) Vu 322 fois
Je repasse pour la réponse sur le primer, en espérant que tu comprends mieux le principe de la méthode Sanger

Bonne journée







 ) C'est pas dit dans le cours, mais tu prendrais un primer complémentaire du brin codant ou non codant, pour accéder directement à la séquence du gène ? On voit ça à la fin ...
) C'est pas dit dans le cours, mais tu prendrais un primer complémentaire du brin codant ou non codant, pour accéder directement à la séquence du gène ? On voit ça à la fin ...






