Salut

Attention de ne pas tout confondre.
On reprend depuis le début:
En premier lieu tu as le benzène qui va subir une substitution. Cette substitution se fera sur n'importe quelle position du benzène car elles sont toutes identiques (le benzène ayant pleins d'axes de symétrie).
Dans ton exemple le benzène sera substitué par un CH3 pour donner le toluène.
Ensuite une fois au stade de toluène, si on veut refaire subir une substitution au toluène, le groupement qui va arriver ne va pas pouvoir se mettre n'importe où car toutes les positions ne sont pas équivalente à cause de la présence du CH3. C'est à partir de ce CH3 que l'on va décrire les position ortho/para et méta.
En effet le groupement CH3 est inductif donneur donc il va enrichir le cycle du benzène en électron.
On aura en plus un effet mésomère au sein du cycle benzénique. Cette mésomérie doit "commencer" quelque part, or tous les carbones du cycle du toluène ne sont pas équivalent car il y en a 1 qui porte le groupement CH3. C'est ce groupement qui lors de la mésomérie va stabilisé le carbocation qui sera donc un carbocation tertiaire, plus stable que les autres qui seront des carbocations secondaires.
Je te remets le schéma pour que tu visualises mieux

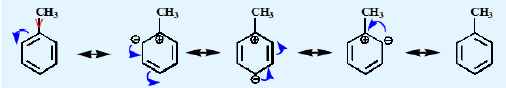
- Capture.PNG (6.71 Kio) Vu 287 fois
Voila si tu bloques encore n'hésite pas à redemander !





 !
! 



