Coucou alors clairement pour le remplissage des cases quantiques par les électrons du carbone je pourrais pas t'expliquer mieux que ce que j'ai fais dans ma fiche, du coup je te mets le screen ici :
Si tu veux plus d'explication en fait va falloir que tu trouves ta réponse dans le premier cours de Chimie G je peux pas t'aider plus perso, et clairement le prof en Chimie O s'en fiche pas mal de cette partie là, c'est pour ça qu'il ne la détaille pas du tout...
Ensuite en ce qui concerne l'hybridation sp3 sp2 et sp, en gros imagine que t'as quatre cases: s ; p ; p ; p
Dans chaque case t'as un électron.
Dans l'hybridation sp3 (sppp) toutes les cases fusionnent pour qu'elles aient toutes la même énergie, donc le carbone peut former 4 liaisons simples avec d'autres atomes.
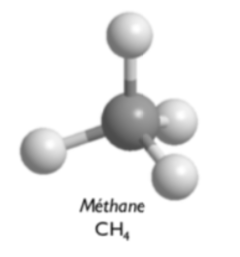
- Capture d’écran 2019-09-03 à 19.31.41.png (24.08 Kio) Vu 242 fois
Dans l'hydridation sp2 (spp), les trois premières cases fusionnent, il reste donc une case p, qu'on appelle p pure !
On a donc trois électrons sp2 qui vont faire des liaisons avec trois autres atomes, et l'électron de la p pure va recouvrir l'une de ces trois liaisons pour former une double liaison ! (C'est un système pi)
Dans l'hydridation sp, les deux premières cases fusionnent, il reste donc deux cases p, qu'on appelle p pures !
On a donc deux électrons sp qui vont faire des liaisons avec deux autres atomes, et les deux électrons des p pures vont recouvrir l'une de ces deux liaisons pour former une triple liaison ! (C'est un double système pi)
Ou alors chaque p pure va recouvrir une liaison simple et on formera deux doubles liaisons !
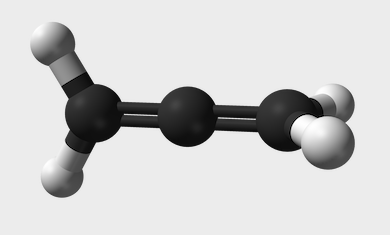
- Capture d’écran 2019-09-03 à 19.39.40.png (31.81 Kio) Vu 242 fois
Est ce que c'est bon pour toi ?








 CHEF TUT ORIENTATION 2020-2021
CHEF TUT ORIENTATION 2020-2021 

 TUTEUR DE CHIMIE ORGA 2019-2020
TUTEUR DE CHIMIE ORGA 2019-2020 


 Ronéiste de BIOPHYSIQUE 2019-2020
Ronéiste de BIOPHYSIQUE 2019-2020 


 Tutrice d'histologie 2019-2020
Tutrice d'histologie 2019-2020 