Salut,
Alors déjà première chose à faire, regarde si on n'a pas représenté certaines choses volontairement comme des hydrogènes lié aux carbones et azotes (aux atomes en général, tu sais qu'un carbone fait 4 liaisons si il en a que 3 c'est qu'il en manque une, c'est celle avec un hydrogène, si l'azote fait que deux liaisons alors qu'il en fait 3 normalement, c'est qu'il est lié à un hydrogènes en plus ...) ou encore des doublets non-liants sur l'azote, l'oxygène, le soufre, le chlore ......
Ensuite, détermine la VSEPR de l'atome auquel on te demande l'hybridation. Donc si lié à 4 atomes AX4, si lié à 3 atomes et un doublets non-liant AX3E, si lié à 2 atomes et 2 doublets non-liants AX2E2 ...
Maintenant il y a 2 possibilités:
-Soit on parle d'un carbone ou d'un autre atomes (O, N) avec un DOUBLET NON-LIANT non délocalisé : dans ce cas il suffit de faire la somme des atomes auxquels il est lié + le nombre de doublets non-liants
-1 (ce que tu as déterminé grace à ta VSEPR) et tu trouves son hybridation.
Par exemple ici :
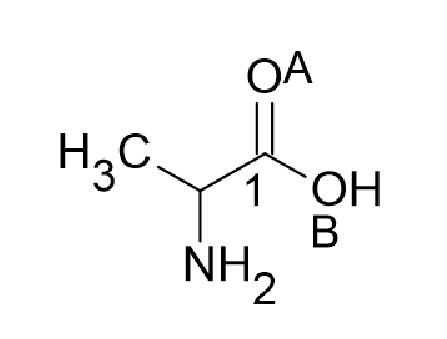
L'atome de carbone 1 possède une VSEPR AX3 (car lié à 3 atomes mais un avec une double liaison (rappel une double liaison, triple ou simple vallent comme 1 en VSEPR), donc a pour hybridation sp2 car 3(nombre d'atomes liés) + 0(doublet non-liant)
-1 = 2 --> donc ton carbone 1 est hybridé sp2, avec 3 orbitales hybrides + 1 p pure pour faire la double liaison
L'atome d'azote, possède un doublet non-liant (pas représenté) et 3 liaisons donc AX3E. On n'a pas de mésomérie avec le doublet non-liant de l'azote car pas de n-sigma -pie (ici un n-sigma-sigma-pie mais ça ne marche pas) donc on peut faire comme au-dessus, 3(nombre d'atomes liés) + 1(nombre de doublet non-liant)
-1= 3 --> donc ton azote est hybridé sp3, avec 4 orbitales hybrides
- Capture d’écran 2022-11-05 175034.png (7.48 Kio) Vu 466 fois
-Soit on parle d'un atome avec un doublet non-liant qui participe à une mésomérie (délocalisé) : dans ce cas on fait : atomes auxquels il est lié + le nombre de doublets non-liants
-2.
Pourquoi ?
Car pour que ce doublet non-liant soit délocalisé, il faut qu'il soit dans une p pure qui a pris la place d'une orbitale hybride, d'où le -2 et pas -1
Comme ici:
L'atome d'oxygène B possède 2 atomes liés + 2 doublets non-liants (pas représentés) donc AX2E2. Ici le doublet non-liant participe à une mésomérie car on a le schéma n-sigma-pie disponible, donc on utilise la deuxième méthode : 2(nombre d'atomes liés) + 2(nombre de doublet non-liant)
-2 = 2 --> donc ton atome d'oxygène B est hybridé sp2, il possède 3 orbitales hybrides et une p pure avec un doublet non-liant qui va se délocaliser !

- Capture d’écran 2022-11-05 175034.png (7.48 Kio) Vu 466 fois
C'est plus clair ?


