Hello hello
 désolé pour l'attente je n'avais pas mon ordi
désolé pour l'attente je n'avais pas mon ordi 
Donc je vais essayer de répondre à toutes tes questions !

Jad'duction a écrit: je ne comprends pas pourquoi l'iode n'est pas en antipériplanaire avec un hydrogène ? Pourquoi on ne pourrait pas avoir un hydrogène lié au même carbone, et en avant ?
Ici en fait tu as ton H qui est comme l'iode, en ARRIERE du plan. Donc ils sont en
syn (=même plan) périplanaire.
Jad'duction a écrit:Et aussi, les E2 sont bien les seules réactions pour laquelle c'est obligatoire que l'hydrogène et le groupement partant soient en antipériplanaire ?
Pour une E2 il faut OBLIGATOIREMENT être en ANTI périplanaire !!
- E1 : on a pas besoin d'être en ANTIpériplanaire car on passe par un carbocation PLAN
- SN
2 : On a une SN en
ANTI aussi mais là c'est différent, ce n'est pas une élimination

Du coup pour en revenir à ce que je disais : là l'hydrogène, sur la molécule qui t'es proposée n'est
PAS en ANTI.
 Mais qui est en ANTI du coup ???
Mais qui est en ANTI du coup ???En anti, tu as le C
3H
7 ici
(un en avant et l'autre à l'opposé = en anti donc en arrière) qui est en avant du plan et l'iode en arrière, ils sont dans des plans
OPPOSES = ANTI Juste en dessous :
 Mais alors comment faire ???
Mais alors comment faire ???Tu dois faire
tourner la molécule comme ceci pour le placer en ANTI :
Désormais ton H est bien en anti => en avant du plan, mais tu remarques que
ta molécule a changé de forme
Attention : le fait que la molécule change de forme est très important car elle détermine si ton alcène sera plutôt E ou Z donc il faut y veiller attention Jad'duction a écrit:D'ailleurs, est-ce que l'hydrogène partant peut se situer sur toute la molécule, ou doit rester assez proche du groupement partant ?
Alors petit rappel :
- Lorsque l'iode s'en va il va voler l'électron du carbone auquel il est lié = formation d'un C+ (il va vouloir récupérer son électron)
- Lorsque l'H s'en va il va donner son électron au carbone pour partir sous forme d'H+ (proton) = formation d'un C- (carbanion)
Un carbanion C- est en surcharge électronique > il va vouloir donner son électron en trop
Tu te retrouves donc avec ceci :
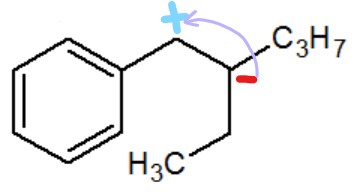
- react 3.jpg (10.87 Kio) Vu 372 fois
Tu fais bien attention que la molécule a changé de forme de manière à placer l'H en anti et pouvoir réaliser l'E2, c'est le résultat de la rotation de tout à l'heure Face à ceci tu te dis "
mais ça tombe bien, on a un C+ qui veut 1 électron qui est juste à côté d'un C- qui veut en donner 1"
C'est exactement ça qu'il va se passer pour former la DL :
- Le C- va donner son électron en trop au C+
- Les 2 carbones seront chargés correctement mais il leur restera un électron célibataire chacun
- Ils vont ainsi mettre chacun leur électron célibataire en commun pour former la 2e barre de la double liaison
Rappel : une liaison est l'association de 2 émectrons venant de 2 atomes
Donc
OUI :
il est nécessaire d'éliminer un H accroché à un C qui soit situé à 1 SEULE liaison du C auquel est lié l'iode (de manière à ce que C- et C+ soient seulement séparés d'une liaison.
PS : ici c'est une E2, la réaction se déroule
trop rapidement = on a pas le temps de passer par un intermédiaire "
fixe" C+ ou C-, donc quand je t'en parle c'est pour expliquer le processus, mais retiens ça :
PAS D'INTERMEDIAIRE REACTIONNEL CARBOCATION DANS LES REACTIONS DE TYPE 2 C'est bon pour toi ??








