Salut !
Déjà il faut savoir que ça sera toujours un site nucléophile (riche en électrons) qui attaque un site électrophile (pauvre en électrons) et pas l'inverse, voilà l'explication de l'item faux. Ensuite, il faut voir que dans une carbonyle, l'oxygène étant très électronégatif va attirer les électrons de la liaison vers lui au dépend du carbone, créant ainsi un site électrophile (le carbone) et un site nucléophile (l'oxygène), cependant comme en réactivité du carbone on se fixe sur ce dernier, on dira que le carbonyle est électrophile. On pourra donc avoir des molécules nucléophiles qui dans certaines réactions vont pouvoir attaquer le carbonyle, au niveau du carbone.
(Comme par exemple dans ce mécanisme, pas à savoir)
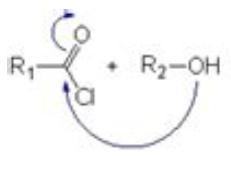
- Capture d’écran 2022-12-11 164509.png (21.57 Kio) Vu 450 fois
J'espère que c'est plus clair
Bonne soirée !


