Coucou !
Je me suis renseigné sur la molécule, j'ai rarement vu ce genre de configuration, surtout en annales, donc je ne pense pas que ça tombe, mais comme ça tu peux comprendre.
En fait, dans cette molécule, on a un carbone qui est lié à un oxygène et deux souffre, tous les deux lié à un hydrogène chacun, d'où le fait qu'ils soient entre parenthèses ensemble.
Donc on a un carbone lié par une double liaison à l'oxygène vers le haut, et lié par une simple liaison à un soufre de chaque côté. Chaque souffre est aussi lié à un hydrogène de chaque côté. On a donc développé la molécule pour avoir une idée de ce à quoi elle ressemble, mais on n'a pas idée des DNL pour le moment, et pour les connaître il faut aussi connaître les numéros atomiques des atomes composant la molécule (ces atomes sont croisés fréquemment) : Souffre : 16 --> 1s2 2s2 2p6 3s2 3p4 --> valence : 6e- ; Carbone : 6 --> 1s2 2s2 2p2 valence : 4e- (on n'oublie pas la valence secondaire sp3 qui lui permettra de faire 4 liaisons) ; Hydrogène : 1 --> 1s1 --> valence : 1e-; Oxygène : 8 --> 1s2 2s2 2p4 --> valence : 6e-.
On s'intéresse maintenant à la VSEPR des atomes chacun leur tour, mais maintenant qu'on a décomposé ça va être beaucoup plus facile : l'oxygène est lié au carbone seulement par une double liaison, donc AX1, et fait 2 DNL puisqu'il a 4 électrons non utilisés donc E2 (ici le piège était qu'il est lié à 1 atome par une double liaison, donc seulement AX1 parce qu'on se demande le nombre d'atomes pour le X).
L'atome de souffre, il y en a un de chaque côté mais notre molécule est symétrique donc ils ont la même VSEPR, il est lié à un carbone d'un côté et un hydrogène de l'autre par des simples liaisons, donc il a 2 DNL car il lui reste 4 e- de valence. Donc sa VSEPR est AX2E2.
Pour moi, le carbone est bien hybridé sp3 comme dit plus haut, mais le souffre n'a pas à être hybridé car il a 4 e- sur sa sous couche p donc ça n'aurait pas d'intétêt, il ne serait pas plus stable avec 5e- en p et 1 en s.
Je dirais donc item E.
Je t'ai fait un (terrible, je suis pas une artiste désolée mdr) dessin pour que tu puisses imaginer la molécule avec tous les DNL en violet.
Voilà, sans la correction je ne peux pas m'assurer que je ne te dis pas de bêtises, mais après y avoir bien réfléchi je pense que c’est comme ça qu'il fallait répondre à ce QCM ! N'hésites pas si tu n'as pas compris, et je veux bien que tu me confirmes que c’est la réponse E si tu as la correction !
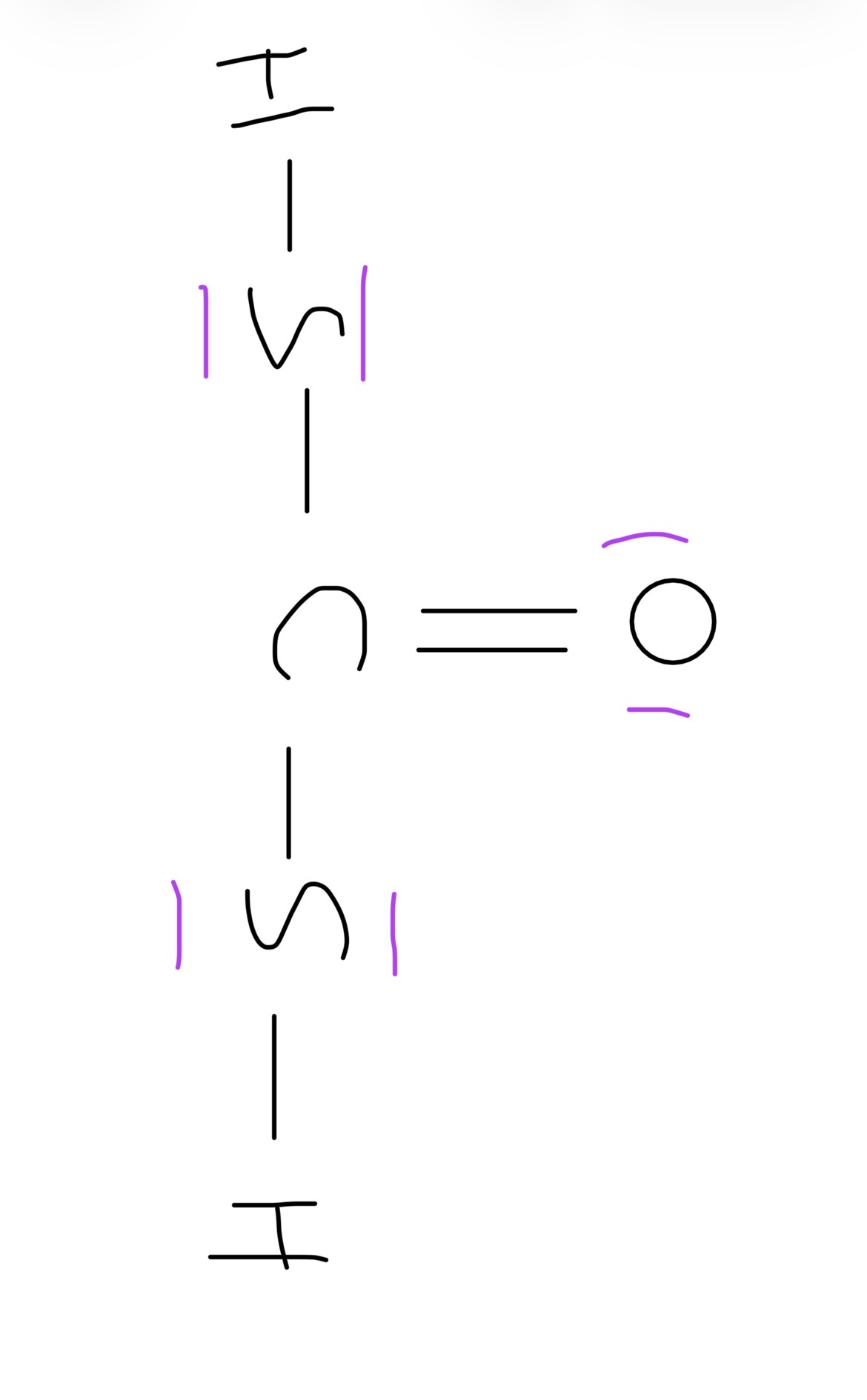
- IMG_0124.jpg (63.12 Kio) Vu 50 fois


