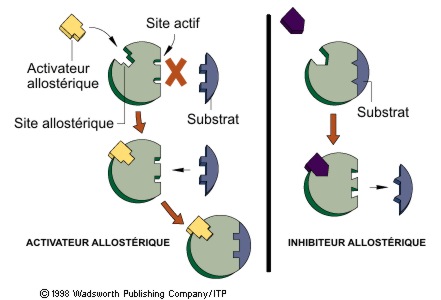
L'enzyme allostérique homotrope a des protomères avec chacun un site de régulation et un site actif (=site de fixation + site catalytique).
Mais dans les homotropes on peut dire que (selon le modèle de la serrure) le site de régulation à la meme forme que le site catalytique donc il peuvent fixer la meme molécule (le substrat)
Pour les allostériques en générale est-ce que la "puissance" d'affinité est proportionelle au nombre d'effecteurs fixés? Il en suffit d'un pour activer l'octamere mais si il y en a plus c'est encore plus efficace ?
ça je pense qu'on le verra plus tard mais bon : est-ce que le produit d'une voie métabolique agit comme un effecteur négatif sur l'enzyme allostérique ?
Voilà merci au courageux qui répondront