Squeeze! a écrit:Hello !

J'ai un problème avec un QCM, je ne vois pas du tout comment il faut s'y prendre =s
Est-ce que quelqu'un peut m'éclairer ?
On donne la distance d(O-H) = 10^-10 m et un angle de 104° pour la molécule d'eau.
Le moment dipolaire de la molécule d'eau a pour valeur ( en C.m ) :
A 1,6.10^-29
B 3,2.10^-29
C 2,3.10^-29
D 1,6.10^-27
E 6,2.10^-30
(Au cas où des gens se poseraient encore des questions sur ce QCM...)En préparant la tut' rentrée, j'ai eu un petit déclic

(mon cerveau se remet petit à petit en route

).
En fait, ce QCM est faux... La réponse E est vraie, mais elle ne correspond pas aux données...
Le seul calcul approximatif que l'on peut faire est le suivant :
le barycentre des charges positives se trouve exactement entre les 2 atomes d'hydrogène.
Donc la distance entre les 2 barycentres serait
)
On trouverait donc

Or, ce résultat est très éloigné du moment dipolaire réel de la molécule d'eau

.
Pourquoi ? Tout simplement parce que dire que la charge totale est de

est déjà une approximation, mais surtout parce que la distance réelle entre les 2 barycentres est bien plus petite (les charges positives et négatives sont attirées entre-elles !).
Donc lorsque l'on demande de calculer le moment dipolaire
d'une molécule avec la formule
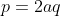
, des approximations sont faites, et il faut en tenir compte dans les réponses proposées... (et donc la réponse réelle devient fausse dans ce cas là

)
Le but de celle/celui qui a fait ce QCM était sans doute de faire perdre du temps à ceux qui faisaient le calcul par rapport à ceux qui avaient appris le résultat par cœur, et d'obliger les étudiants à connaitre le résultat par cœur, mais le QCM en devient annulable selon moi

Bonne soirée à tous, et bon courage aux bosseurs
