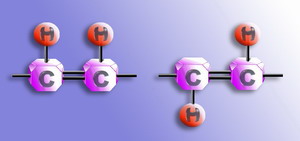
Configuration Trans ça veut dire que les groupements de part et d'autre de la double liaison sont dans des positions inversées !
Dans le cas de la liaison peptidique, tu as de part et d'autre de la liaison (qui est une liaison double partielle):
- d'un côté : le O et le C alpha de l'AA1
- de l'autre : le H de l'amine et le C alpha de l'AA2
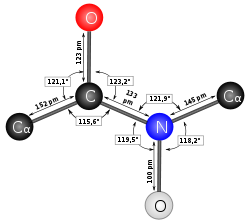
- 250px-Liaison_peptidique.png (14.98 Kio) Vu 782 fois

Sont en trans :
- le O par rapport au H
- les deux C alpha k'un vis à vis de l'autre
On ne peut pas dire que les chaîne lat sont en trans ! Ce n'est pas correct puisque ce ne sont pas des groupements portés par la double liaison ! ça n'aurait aucun sens, ou alors c'est un abus de langage !
La liaison peptidique qui unit le N d'un amine et le C d'un carboxyle est rigide ! Il n 'y a aucune rotation possible autour de cette liaison !
Par contre les laisions qui lient le C apha et le N de l'amine d'un côté
et le C alpha au C du carboxyle de l'autre

sont des liaisons dont la rotation est libre ! les chaines latérales peuvent s'orienter de plusieurs manière : c'est comme tu le dis des conformations différentes et c'est absolument comparable aux isomères de conformation...
...Mais tu as aussi vu sûrement que toutes les conformations ne sont pas équivalentes en terme d'énergie et de stabilité ! Ce qui fait que :
- dans un feuillet béta : les chaines lat vont s'orienter de manière haut-bas-haut-bas-haut-bas... C'est plus stable
- dans les hélices alpha : les chaines lat s'orientent toutes vers l'extérieur de la chaine donc de la même manière mais comme tu as un angle du à la forme de l'hélice, les chaines latérales ne se gênent pas.
Tu as compris ?