Le Guide pour bien débuter la LAS : Ici
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
Tutoriel Forum : Ici
Planning des Séances Tutorat et EB : ICI !
Errata : Séances Tutorat et EB, Annatuts, Ronéos
Centres de Téléchargement : ICI !
Réponses des Profs : ICI !
Annales : Achat, Corrections Officieuses
Annatuts : 2025-2026, Sommaire
MCC 25/26 : ICI
Candidature MMOPK : ICI
Terminale Santé : ICI
GROUPES ET INFOS ATELIERS RENFORCES : Ici
INSCRIPTIONS ENTRETIENS TUTEURS : Ici
Newsletter : ICI
[Résolu] QCM 14
11 messages
• Page 1 sur 1
[Résolu] QCM 14
Bonsoir, je ne comprends pas pourquoi l'item B du QCM 14 est compté faux. Si quelqu'un peut m'aider. Ou me donner un exemple pour une délocalisation d'électrons ne faisant pas dans une orbitale p pure. Merci =)
- Mounir
- Carabin débutant
- Messages: 44
- Inscription: 07 Aoû 2011, 15:43
Re: QCM 14
Pareil pour moi je vois pas 

" Les animaux sont comme des bêtes. D’où leur nom. Ne possédant pas une intelligence supérieure,
ils passent leur temps à faire des bulles ou à jouer dans l’eau au lieu d’aller au bureau. " Desproges
ils passent leur temps à faire des bulles ou à jouer dans l’eau au lieu d’aller au bureau. " Desproges
-

Cédric - Apprenti Carabin
- Messages: 110
- Inscription: 05 Mar 2012, 22:00
Re: QCM 14
tout a faiit d'accord avec toi ... +1 
Soyons optimistes: la médecine a découvert beaucoup plus de remèdes qu'il n'y a de maux.
- flipperDay
- Carabin débutant
- Messages: 20
- Inscription: 11 Sep 2012, 23:49
Re: QCM 14
Salut,
Ben en fait, c'est ton con... Quand t'as un doublet non liant sur une orbitale s, il se délocalise et c'est pas une orbitale p pur
Ben en fait, c'est ton con... Quand t'as un doublet non liant sur une orbitale s, il se délocalise et c'est pas une orbitale p pur

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: QCM 14
Salut !
Attention raboucho, un doublet non-liant ne peut se situer dans une orbitale s !
Pour répondre à mounir :
Je suis un peu désolé du piège, je me rends compte qu'il était vraiment vicieux !
Les électrons délocalisés se situent dans une orbitale "p pure" OU π.
"p pure" pour les DNL, π pour les liaisons doubles.
Ce qu'il fallait voir, c'était que l'orbitale π est différente de l'orbitale "p pure" (de par sa forme et son énergie). Donc même si une orbitale π est construite à partir de deux orbitales "p pures", on ne peut dire que les électrons se situent dans ce dernier type d'orbitale (un peu comme si je disais : un mur est construit à partir d'un tas de briques, mais un tas de briques seul ne constitue pas un mur).
Mais sincèrement c'était un peu limite, c'est une subtilité qu'on ne vous demandera sans doute pas au concours…
Quoi qu'il en soit, continuez comme ça et n'hésitez surtout pas lorsque des doutes de ce type vous apparaissent !
Attention raboucho, un doublet non-liant ne peut se situer dans une orbitale s !
Pour répondre à mounir :
Je suis un peu désolé du piège, je me rends compte qu'il était vraiment vicieux !
Les électrons délocalisés se situent dans une orbitale "p pure" OU π.
"p pure" pour les DNL, π pour les liaisons doubles.
Ce qu'il fallait voir, c'était que l'orbitale π est différente de l'orbitale "p pure" (de par sa forme et son énergie). Donc même si une orbitale π est construite à partir de deux orbitales "p pures", on ne peut dire que les électrons se situent dans ce dernier type d'orbitale (un peu comme si je disais : un mur est construit à partir d'un tas de briques, mais un tas de briques seul ne constitue pas un mur).
Mais sincèrement c'était un peu limite, c'est une subtilité qu'on ne vous demandera sans doute pas au concours…
Quoi qu'il en soit, continuez comme ça et n'hésitez surtout pas lorsque des doutes de ce type vous apparaissent !
Tuteur de chimie orga 2012-2013 retraité
VP G33K et VP Communication
BDE Médecine Nice 2013-2014
π-Carabins
Cliquez pour vous détendre.
VP G33K et VP Communication
BDE Médecine Nice 2013-2014
π-Carabins
Cliquez pour vous détendre.
-

WatiGG - Administrateur

- Messages: 1356
- Inscription: 13 Sep 2010, 19:33
Re: QCM 14
Ce que je ne comprend pas c'est que la question était : " les électrons délocalisés par mésomérie sont toujours situés dans une orbitale p pure" et vous dîtes que non ils peuvent également être dans des orbitales Pi mais dans ce sujet : viewtopic.php?f=332&t=23015
Vous avez écris
"Q9_ Les orbitales π sont elles toujours formées par le recouvrement de deux orbitales p "pures" (= non hybridées) ?
R9_ Tout à fait ! Une orbitale π (intervenant dans les liaisons doubles et triples) est bel et bien issue du recouvrement latéral de deux orbitales p pures, c'est à dire non hybridées avec une orbitale s."
Donc je ne comprend pas pourquoi l'item est faux vu que les orbitales pi sont constituées d'orbitales p pures, on peut dire que les électrons délocalisés par mésomérie sont toujours situés dans une orbitale p pure selon moi.
Vous avez écris
"Q9_ Les orbitales π sont elles toujours formées par le recouvrement de deux orbitales p "pures" (= non hybridées) ?
R9_ Tout à fait ! Une orbitale π (intervenant dans les liaisons doubles et triples) est bel et bien issue du recouvrement latéral de deux orbitales p pures, c'est à dire non hybridées avec une orbitale s."
Donc je ne comprend pas pourquoi l'item est faux vu que les orbitales pi sont constituées d'orbitales p pures, on peut dire que les électrons délocalisés par mésomérie sont toujours situés dans une orbitale p pure selon moi.
-

Mister Orrange - Carabin Geek
- Messages: 506
- Inscription: 04 Sep 2012, 18:00
Re: QCM 14
Re 
Ben pourtant, si on prend l'azote : 1s2 2s2 2p3
On a bien le dnl sur la s...
Ou on parle pas de la même chose ?
Merci

WatiGG a écrit:Salut !
Attention raboucho, un doublet non-liant ne peut se situer dans une orbitale s !
Ben pourtant, si on prend l'azote : 1s2 2s2 2p3
On a bien le dnl sur la s...

Ou on parle pas de la même chose ?

Merci

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
Re: QCM 14
Non Raboucho tu oublies le fait que les atomes hybrident leurs orbitales atomiques pour former des orbitales hybrides !
On se retrouve avec soit des orbitales sp, soit des orbitales p pures. Le DNL se trouve forcément dans l'une des deux catégories!
(Culture G : exception pour l'hydrogène qui ne dispose pas d'orbitales p à mélanger…)
@Sami : lis l'intégralité de ma réponse …
Pour illustrer :
Voici une orbitale π (en rouge et bleu) :
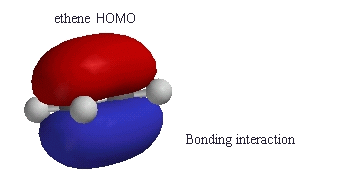
Voici une orbitale p pure :
 (magnifique dessin de crashtest ^^)
(magnifique dessin de crashtest ^^)
Il est donc impossible pour un électron de se trouver à la fois dans une orbitale p pure et dans une orbitale π.
On se retrouve avec soit des orbitales sp, soit des orbitales p pures. Le DNL se trouve forcément dans l'une des deux catégories!
(Culture G : exception pour l'hydrogène qui ne dispose pas d'orbitales p à mélanger…)
@Sami : lis l'intégralité de ma réponse …
WatiGG a écrit:Ce qu'il fallait voir, c'était que l'orbitale π est différente de l'orbitale "p pure" (de par sa forme et son énergie). Donc même si une orbitale π est construite à partir de deux orbitales "p pures", on ne peut dire que les électrons se situent dans ce dernier type d'orbitale (un peu comme si je disais : un mur est construit à partir d'un tas de briques, mais un tas de briques seul ne constitue pas un mur).
Pour illustrer :
Voici une orbitale π (en rouge et bleu) :

Voici une orbitale p pure :
 (magnifique dessin de crashtest ^^)
(magnifique dessin de crashtest ^^)Il est donc impossible pour un électron de se trouver à la fois dans une orbitale p pure et dans une orbitale π.
Tuteur de chimie orga 2012-2013 retraité
VP G33K et VP Communication
BDE Médecine Nice 2013-2014
π-Carabins
Cliquez pour vous détendre.
VP G33K et VP Communication
BDE Médecine Nice 2013-2014
π-Carabins
Cliquez pour vous détendre.
-

WatiGG - Administrateur

- Messages: 1356
- Inscription: 13 Sep 2010, 19:33
Re: QCM 14
Oui c'est vrai, me suis emmêlé les pinceaux désolé 
J'avais oublié qu'après l'hybridation on n'avais plus de s...
En tout cas, merci beaucoup
J'avais oublié qu'après l'hybridation on n'avais plus de s...

En tout cas, merci beaucoup

-

Raboucho - CM Forum
- Messages: 2982
- Inscription: 15 Aoû 2012, 22:01
- Localisation: Donjon Marseillais
11 messages
• Page 1 sur 1
Retourner vers Chimie Organique
Qui est en ligne
Utilisateurs parcourant ce forum: Aucun utilisateur enregistré et 2 invités






 N'oubliez pas de passer votre post en résolu svp
N'oubliez pas de passer votre post en résolu svp