Salut

Je complète la réponse de Raboucho
(merci) par des schémas.
Voilà l'acétylène, une molécule liant deux C par une triple liaison
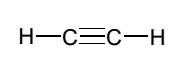
- Acétylène.png (1.05 Kio) Vu 270 fois
D'un point de vue orbitalaire, ça donne ça:
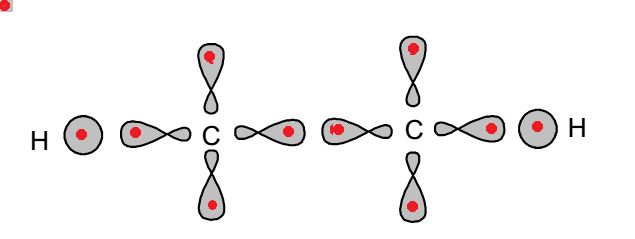
- OA.png (11.63 Kio) Vu 270 fois
Les points rouges correspondent aux électrons, chaque atome donne son électron pour permettre la liaison.
La liaison correspond dc à la mise en commun de 2 électrons.
La liaison sigma, c'est celle du milieu, la plus forte en énergie, la liaison axial
Les liaisons pi, ce sont les liaisons latérales, plus fragiles car plus périphériques, ce sont elles qui casseront lors des réactions d'addition par exemple.
Voilà, j'espère que tu y vois mieux.
Edit: Je viens de voir ton message, je laisse mon post quand même, salut




 oui oui tu m'as bien aidé crois moi haha j'ai réussi à comprendre cette histoire de règle de l'octet et de déplacement d,'electrons mais j'ai encore un peu de mal avec les visualisation des liaisons sigma et pi...
oui oui tu m'as bien aidé crois moi haha j'ai réussi à comprendre cette histoire de règle de l'octet et de déplacement d,'electrons mais j'ai encore un peu de mal avec les visualisation des liaisons sigma et pi... 



 N'oubliez pas de passer votre post en résolu svp
N'oubliez pas de passer votre post en résolu svp 
 merci d'avoir rajouté ton post je pense avoir compris maintenant c'est supeeer haha
merci d'avoir rajouté ton post je pense avoir compris maintenant c'est supeeer haha